Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2. Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
VO2 = 2 . 2 = 4 lít.
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
VCO2 = 0,15 . 22,4 = 3,36 lít.
c) Tỉ khối của khí metan và không khí là:
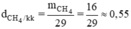
Vậy khí metan nhẹ hơn không khí 0,55.

\(\left\{{}\begin{matrix}C_xH_y:a\left(mol\right)\\CO:b\left(mol\right)\end{matrix}\right.=>a+b=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CO_2}=\dfrac{22}{44}=0,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Bảo toàn C: ax + b = 0,5
Bảo toàn H: ay = 0,8
Bảo toàn O: b + 0,6.2 = 0,5.2 + 0,4
=> b = 0,2 (mol)
=> a = 0,1 (mol)
=> x = 3 ; y = 8 => CTPT: C3H8
\(\left\{{}\begin{matrix}\%V_{C_3H_8}=\dfrac{0,1}{0,3}.100\%=33,33\%\\\%V_{CO}=\dfrac{0,2}{0,3}.100\%=66,67\%\end{matrix}\right.\)

Gọi số mol H2, C2H2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{17,92}{22,4}=0,8\left(mol\right)\\\overline{M}=\dfrac{2a+26b}{a+b}=0,5.28=14\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,4 (mol); b = 0,4 (mol)
\(n_{O_2}=\dfrac{35,84}{22,4}=1,6\left(mol\right)\)
PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
0,4--->1----------->0,8
2H2 + O2 --to--> 2H2O
0,4-->0,2
=> Y gồm \(\left\{{}\begin{matrix}CO_2:0,8\left(mol\right)\\O_{2\left(dư\right)}:0,4\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{CO_2}=\dfrac{0,8}{0,8+0,4}.100\%=66,67\%\\\%V_{O_2}=\dfrac{0,4}{0,8+0,4}.100\%=33,33\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{CO_2}=\dfrac{0,8.44}{0,8.44+0,4.32}.100\%=73,33\%\\\%m_{O_2\left(dư\right)}=\dfrac{0,4.32}{0,8.44+0,4.32}.100\%=26,67\%\end{matrix}\right.\)

a) Gọi số mol H2, CH4 là a, b
=> \(a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(M_X=\dfrac{2a+16b}{a+b}=0,325.32=10,4\)
=> a = 0,2 ; b = 0,3
=> \(\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,2}{0,5}.100\%=40\%\\\%V_{CH_4}=\dfrac{0,3}{0,5}.100\%=60\%\end{matrix}\right.\)
b) \(n_{O_2}=\dfrac{32}{32}=1\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,3--->0,6------->0,3
2H2 + O2 --to--> 2H2O
0,2-->0,1
=> \(\left\{{}\begin{matrix}V_{CO_2}=0,3.22,4=6,72\left(l\right)\\V_{O_2\left(dư\right)}=\left(1-0,6-0,1\right).22,4=6,72\left(l\right)\end{matrix}\right.\)

a)
2CO + O2 --to--> 2CO2
2H2 + O2 --to--> 2H2O
b) \(n_{H_2O}=\dfrac{12,6}{18}=0,7\left(mol\right)\); \(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2CO + O2 --to--> 2CO2
0,6<--0,3<------0,6
2H2 + O2 --to--> 2H2O
0,7<--0,35<------0,7
=> \(\left\{{}\begin{matrix}V_{CO}=0,6.22,4=13,44\left(l\right)\\V_{H_2}=0,7.22,4=15,68\left(l\right)\end{matrix}\right.\)
VO2 = (0,3 + 0,35).22,4 = 14,56 (l)
c) \(M_A=\dfrac{0,6.28+0,7.2}{0,6+0,7}=14\left(g/mol\right)\)
=> \(d_{A/O_2}=\dfrac{14}{32}=0,4375\)

\(n_{CO_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\)
Bảo toàn C: nC = 0,75 (mol)
Bảo toàn H: nH = 2 (mol)
=> \(n_O=\dfrac{23-0,75.12-2.1}{16}=0,75\left(mol\right)\)
nC : nH : nO = 0,75:2:0,75 = 3:8:3
=> CTPT: (C3H8O3)n
Có \(n_{O_2}=\dfrac{m}{32}\left(mol\right)\) => \(n_A=\dfrac{m}{32}.34,78\%=0,01087m\left(mol\right)\)
=> \(M_A=\dfrac{m}{0,01087m}=92\left(g/mol\right)\)
=> n = 1
=> CTPT: C3H8O3

Gọi thể tích CO và CO2 lần lượt là x và y (ml)
Tổng thể tích hỗn hợp trộn là:
V = VX + Vkk = 50 + 200 = 250 (ml)
VO2 = 20% . 200 = 40 (ml)
=> VN2 = 200 - 40 = 160 (ml)
%VN2 bđ = VN2 / V . 100% = 160/250 . 100% = 64%
PTPƯ:
2CO + O2 --to--> 2CO2
x ---------> x/2 ---------> x
Tổng thể tích hỗn hợp sau PƯ:
V’ = VCO2 (ban đầu + sau pư) + VO2 còn lại + VN2 (không đổi)
= (x + y) + (40 - x/2) + 160 = 200 + x/2 + y (ml)
%VN2 sau pư = 160/(200 + x/2 + y) . 100% = 64% + 3,36% = 67,36%
Ta có hpt:
x + y = 50;
160/(200 + x/2 + y) . 100% = 67,36%
=> x ≈ 25 (ml)
=> %VCO = 25/50 . 100% = 50%
V nước = = 1250 - 550 = 700(ml)
V nio = 100(ml)
=> V CO2 = 550 - 250 = 300(ml)
Bảo toàn nguyên tố với N :
=> V NH3 = 2 V N2 = 200(ml)
=> V hidrocacbon = 300 -200 = 100(ml)
Ta có :
Số nguyên tử C = V CO2 / V hidrocacbon = 300/100 = 3
Khi đốt NH3, V H2O sinh ra = 3/2 V NH3 = 300(ml)
=> V H2O khi đốt hidrocacbon sinh ra = 700 -300 = 400(ml)
Số nguyên tử H = 2V H2O / V hidrocacbon = 400.2/100 = 8
Vậy CTPT của hidrocacbon là C3H8