Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
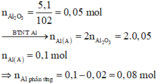
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
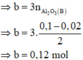
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
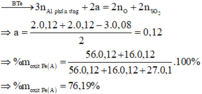

Đáp án D
Dung dịch B mất màu hoàn toàn => Cu2+ phản ứng hết
3 kim loại là Ag, Cu, Fe dư.
mFe dư =55,2-108.0,4-64.0,1=5,6 gam
Đặt số mol Mg và Fe phản ứng lần lượt là x, y
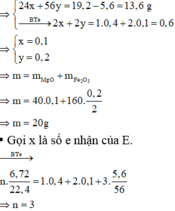
=> Khí E là NO

Hỗn hợp B gồm Cu và Fe dư. nCu = 0,15 mol; nFe = 0,1 - 0,05 = 0,05 mol.
Khi tác dụng với dung dịch HNO3: Theo phương pháp bảo toàn eletron
Chất khử là Fe và Cu
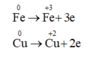
Chất oxi hoá là HNO3
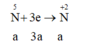
Ta có 3a = 0,15 + 0,3; a = 0,15 (mol),
VNO = 0,15.22,4 = 3,36 (lít)
Đáp án B

Đáp án D
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=>3x + 6z = 2y + 0,15 + 0,1 + 8t(1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=>t + 3x = 2z(2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13(3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=>1,36 = 32z – 16.(1,5x – y)(4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g

Giải thích:
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=> 3x + 6z = 2y + 0,15 + 0,1 + 8t (1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=> t + 3x = 2z (2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13 (3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=> 1,36 = 32z – 16.(1,5x – y) (4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g
Đáp án D
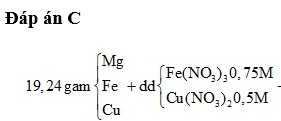
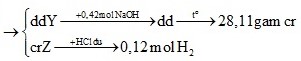


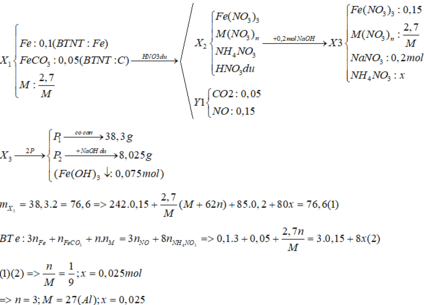
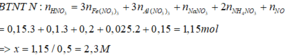
Chia, tách nhỏ từng bài tập, quá trình ra để giải:
chỉ có Al + NaOH → NaAlO2 + 3/2H2
nNaOH = nH2 = 0,12 mol
⇒ chứng tử sau phản ứng NaOH còn dư 0,04 mol và ∑nAl trong A = 0,08 mol.
Khí B như ta biết gồm CO2 (sinh ra do FeCO3) và H2 (do Fe)
10 gam kết tủa là 0,1 mol CaCO3
⇒ có 0,1 mol CO2 ⇒ nFeCO3 = 0,1 mol.
Rắn R ra chắc chắn có Cu và có thể là còn dư kim loại Fe. Vậy phần trong dung dịch?
À, gồm: 0,08 mol AlCl3; 0,12 mol NaCl + ??? mol FeCl2. Mà ∑nHCl = nHCl = 0,74 mol
⇒ bảo toàn Cl có ngay nFeCl2 = 0,19 mol; sinh ra do 0,1 mol FeCO3 ⇒ còn 0,09 nữa do Fe.
Vậy mR = mCu, Fe lọc ra = 20 – mAl – mFeCO3 – mFe phản ứng = 1,2 gam.
R gồm Cu, Fe là các kim loại hoạt động TB yếu nên + HNO3 sinh NO hoặc NO2.
ở đây dùng HNO3 đặc nên khí duy nhất sinh ra là NO2 |
nNO2 = 0,05 mol
⇒ bảo toàn electron có 3nFe + 2nCu = nNO2 = 0,05 mol mà mFe + Cu = 1,2 gam
⇒ giải ra nFe = nCu = 0,01 mol. Đọc tiếp quá trình cuối
⇒ m gam sản phẩm gồm 0,01 mol CuO và 0,05 mol Fe2O3 ⇒ m = 1,6 gam
Đáp án B