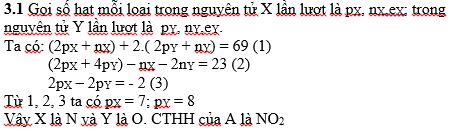Nhiệt phân muối Cu(XY3)2 hoặc muối AgXY3 đều thu đc khí A sau sơ đồ phản ứng sau:
Cu(XY3)2->CuY+XY2+Y2
AgXY3->Ag+XY3+Y3
Nhiệt phân a gam Cu(XY3)2 thu đc V1 lít hh khí, b gam AgXY3 thu đc V2=1,2V1 lít hh khí
a. Viết PTHH, xác định tỉ lệ a/b biết phản ứng xảy ra hoàn toàn cung đk nhiệt độ và áp suất
b. Tính V1 và V2 ở đktc nếu a=56,4g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
Theo bài:
\(2p_X+n_X+2\left(2p_Y+n_Y\right)=69\)
\(\Leftrightarrow2\left(p_X+2p_Y\right)+\left(n_X+2_Y\right)=69\left(1\right)\)
\(2\left(p_X+2p_Y\right)-\left(n_X+2n_Y\right)=23\left(2\right)\)
\(\left(1\right)+\left(2\right)\Rightarrow\left\{{}\begin{matrix}p_X+2p_Y=23\left(3\right)\\n_X+2n_Y=23\end{matrix}\right.\)
Mà \(-2p_X+2p_Y=2\left(4\right)\)
\(\left(3\right)+\left(4\right)\Rightarrow\left\{{}\begin{matrix}p_X=7\left(N\right)\\n_Y=8\left(O\right)\end{matrix}\right.\)
Vậy khí A là NO2

\(n_{HCl}=\dfrac{58,4.15\%}{36,5}=0,24\left(mol\right)\\ Fe+2HCl\rightarrow\left(t^o\right)FeCl_2+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,24}{2}=0,12\left(mol\right)\\ \Rightarrow V1=V_{H_2\left(đktc\right)}=0,12.22,4=2,688\left(l\right)\\ x=m_{Cu}=m_{hhA}-m_{Fe}=15,68-0,12.56=8,96\left(g\right)\\ b,n_{Cu}=\dfrac{8,96}{64}=0,14\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Cu+Cl_2\rightarrow\left(t^o\right)CuCl_2\\ n_{Cl_2}=\dfrac{3}{2}.n_{Fe}+n_{Cu}=\dfrac{3}{2}.0,12+0,14=0,32\left(mol\right)\\ \Rightarrow V2=V_{Cl_2\left(đktc\right)}=0,32.22,4=7,168\left(l\right)\\ y=m_{muối}=m_{AlCl_3}+m_{CuCl_2}=0,12.133,5+0,14.135=34,92\left(g\right)\)

Cho hỗn hợp pư với HCl,chỉ có Mg pư vì Mg đứng trước H trong dãy hoạt động hóa học.Vậy khí A là H2,dd C là MgCl2, chất rắn B là Cu và Ag
mMg=10.14 -1.54=8.6g
nH2= 7.48/22.4=\(\frac{187}{560}\)
PT: Mg +2HCl ----> MgCl2 + H2
\(\frac{187}{560}\) \(\frac{187}{560}\)
mMgCl2= \(\frac{187}{560}\) *95=31.72g

Al, Fe không tác dụng với H2SO4 đặc nguội
Rắn không tan ở TN2 là Cu
mCu = 6,4 (g)
=> \(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,1-------------------------->0,1
=> V = 0,1.22,4 = 2,24 (l)

Đây chỉ là một bài toán về kim loại Cu tác dụng với dung dịch có chứa NO3- và H+ đơn giản.
Để giải quyết bài này ta chỉ cần sử dụng đến phương trình ion thu gọn để giải quyết.
Thí nghiệm 1: ta có:
![]()
Xét phản ứng: 3Cu + 2NO3- + 8H+ → 3 C u 2 + +2NO + 4 H 2 O
Ban đầu: 0,12 (mol) 0,16 0,16
Phản ứng: 0,06 0,04 0,16 0,04
Sau phản ứng: 0,06 0,12 0 0,04
Thí nghiệm 2: ta có:
![]()
Xét phản ứng: 3Cu + 2 N O - 3 + 8 H + → 3 C u 2 + + 2NO + 4 H 2 O
Ban đầu: 0,12 (mol) 0,16 0,32
Phản ứng: 0,12 0,08 0,32 0,08
Sau phản ứng: 0 0,08 0 0,08
Ta thấy:
![]()
Đáp án C.