Câu 1 Cho 8,8g hỗn hợp Fe và Cu tác dụng hoàn toàn với dd HCl. Phản ứng xong, thu được 3,2 g chất rắn. Khối lượng của mỗi kim loại trong hỗn hợp Fe và Cu
A.56g và 3,2 g
B.5,6g và 64g
C.5,6g và 3,2g
D.56g và 64g
Câu 2 Có bốn kim loại: X, Y, Z, O đứng sau Mg trong dãy hoạt động hóa học. Biết rằng:
+ X và Y không phản ứng với dung dịch HCl
+ Z và O tác dụng với dung dịch HCl giải phóng khí hiđro.
+ X tác dụng với dung dịch muối của Y và giải phóng Y.
+ O tác dụng với dung dịch muối của Z và giải phóng Z.
Hãy xác định thứ tự sắp xếp các kim loại trên theo chiều hoạt động hóa học giảm dần
A.X, Y, Z, O
B.O ,Z, X, Y
C.X, O, Z, Y
D.Y, X, O, Z
Câu 3 Hoà tan hoàn toàn a gam sắt bằng dung dịch H 2 SO 4 loãng. Thu được 2,24 lít khí hiđro (đktc). Giá trị của a là:
A.5,6 gam.
B.11,2 gam
C.56 gam
D.0,56 gam.

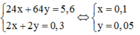
Câu 1 Cho 8,8g hỗn hợp Fe và Cu tác dụng hoàn toàn với dd HCl. Phản ứng xong, thu được 3,2 g chất rắn. Khối lượng của mỗi kim loại trong hỗn hợp Fe và Cu
A.56g và 3,2 g
B.5,6g và 64g
C.5,6g và 3,2g
Chất rắn không tan là Cu (3,2g)
=> Khối lượng Fe: 8,8-3,2=5,6(g)
D.56g và 64g
Câu 2 Có bốn kim loại: X, Y, Z, O đứng sau Mg trong dãy hoạt động hóa học. Biết rằng:
+ X và Y không phản ứng với dung dịch HCl
+ Z và O tác dụng với dung dịch HCl giải phóng khí hiđro.
+ X tác dụng với dung dịch muối của Y và giải phóng Y.
+ O tác dụng với dung dịch muối của Z và giải phóng Z.
Hãy xác định thứ tự sắp xếp các kim loại trên theo chiều hoạt động hóa học giảm dần
A.X, Y, Z, O
B.O ,Z, X, Y
C.X, O, Z, Y
D.Y, X, O, Z
Câu 3 Hoà tan hoàn toàn a gam sắt bằng dung dịch H 2 SO 4 loãng. Thu được 2,24 lít khí hiđro (đktc). Giá trị của a là:
A.5,6 gam.
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
B.11,2 gam
C.56 gam
D.0,56 gam.