Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

* Phương pháp xác định nồng độ phần trăm dung dịch C u S O 4
- Cân một lượng dung dịch C u S O 4 xác định.
- Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng đó là C u S O 4 . Sau đó đem cân lượng muối sau khi cô cạn này ta được số liệu là mct.
- Áp dụng công thức: 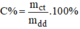 ta sẽ tính C% của dung dịch
C
u
S
O
4
.
ta sẽ tính C% của dung dịch
C
u
S
O
4
.
* Phương pháp xác định nồng độ mol của dung dịch C u S O 4 :
- Đong 1 thể tích dung dịch C u S O 4 xác định, đem cân lượng dung dịch đó.
- Sau đó dùng công thức 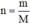 để tính số mol của
C
u
S
O
4
.
để tính số mol của
C
u
S
O
4
.
- Tính nồng độ mol của dung dịch
C
u
S
O
4
bằng công thức: 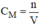

Refer.
Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
\(C\%=\dfrac{8}{100}\cdot100\%=8\%\)
Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
\(n_{CuSO_4}=\dfrac{8}{160}=0.05\left(mol\right)\)
– Tính nồng độ mol của dung dịch CuSO4 :
\(C_M=\dfrac{1000\cdot0.05}{90}=0.56\left(M\right)\)

Bài 1: Bạn tự học nhé
Bài 2:
\(C_M=\dfrac{n}{V}=\dfrac{2,5}{4}=0,625M\)
Bài 3:
\(a,CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\\ b,SO_3+H_2O\rightarrow H_2SO_4\)
Bài 4:
a, HNO3 - axit nitric
Ca(OH)2 - canxi hiđroxit
b, K2SO4
NaHCO3
mình làm nốt bài 1 :)))
oxit là 1 hợp chất trong đó có 1 hay nhiều nguyên tử Oxi liên kết với 1 đơn chất
VD : CO2 , FeO

5 Nồng độ phần trăm là gì? Trong hóa học, nồng độ phần trăm của dung dịch được kí hiệu là C% cho ta biết số gam chất tan có trong 100 gam dung dịch là bao nhiêu
C%=\(\dfrac{20}{620}.100=3,22\%\)
CM=\(\dfrac{1,5}{0,75}\)=2M
6 ko giải thích lại
C%=\(\dfrac{30}{230}100=13\%\)
CM=\(\dfrac{1}{0,2}\)=5M

Ta có: V A : V B = 2:3
Số mol H 2 S O 4 có trong 2V (l) dung dịch A:
n H 2 S O 4 = C M . V A = 0,2 . 2V = 0,4V (mol)
Số mol H 2 S O 4 có trong 3V (l) dung dịch B:
n H 2 S O 4 = C M . V B = 0,5 . 3V = 1,5V (mol)
Nồng độ mol của dung dịch H 2 S O 4 sau khi pha trộn:
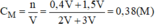
Vậy nồng độ mol của dung dịch C là 0,38M.

Đổi 100 ml = 0,1 l
Ta có: nCuSO4 = \(\dfrac{m}{M}=\dfrac{8}{64+32+16.4}=0,05mol\)
Nồng độ mol của CuSO4:
\(\Rightarrow\) \(C_{MddCuSO_4}=\dfrac{n}{V}=\dfrac{0,05}{0,1}=0,5M\)
Mà: \(m_{ddCuSO_4}=m_{CuSO_4}+m_{H_2O}\) = \(8+100=108\left(g\right)\)
Nồng độ phần trăn dung dịch CuSO4 là:
\(\Rightarrow C\%_{ddCuSO_4}=\dfrac{m_{ct}}{m_{dd}}.100\%=\dfrac{8}{108}.100\%\approx7,4\%\)

1. Dung dịch CuSO4 có nồng độ 0,5mol/lit là trong 1 lít dung dịch CuSO4 thì chứa 0,5 mol CuSO4
2. Dung dịch đường có nồng độ 2 mol/lit cho biết trong 1 lít dung dịch đường thì chứa 2 mol đường
3. \(CM_{NaCl}=\dfrac{n}{V}=\dfrac{0,75}{4}=0,1875M\)
4. \(n_{NaOH}=\dfrac{16}{40}=0,4\left(mol\right)\\ CM_{NaOH}=\dfrac{0,4}{0,2}=2M\)
trình bày phương pháp thực nghiệm để xác định nồng độ % và nồng độ mol của một mẫu thử dung dịch CuSO4
Trả lời
a) Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
C%=100%×8100=8%C%=100%×8100=8%
b) Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
nCuSO4=8160=0,05(mol)nCuSO4=8160=0,05(mol)
– Tính nồng độ mol của dung dịch CuSO4 :
CM=1000×0,0590≈0,56(mol/l)
a) Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
C% = (100%×8):100=8%
b) Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
\(_{n_{CuSO4}}\) = 8:160=0,05(mol)
– Tính nồng độ mol của dung dịch CuSO4 :
\(_{C_M}\)= (1000×0,05) : 90 ≈ 0,56(mol/l)