Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Ca có 2 electron ở lớp ngoài cùng (giống như nguyên tử Mg) => Dễ dàng cho đi 2 electron ở lớp ngoài cùng để tạo cấu hình electron bền vững của khí hiếm
- O có 6 electron ở lớp ngoài cùng => Dễ dàng nhận thêm 2 electron ở lớp ngoài cùng để tạo cấu hình electron bền vững của khí hiếm
Cái sơ đồ em vẽ vòng e của 2 nguyên tử dùng dấu + xong -> thành 2 vòng e các nguyên tử sát nhau

Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
Từ đây em tự vẽ khi mỗi nguyên tử góp 1e dùng chung

- Phân tử potassium chloride là hợp chất ion được tạo bởi kim loại điển hình (K) và phi kim điển hình (Cl)
- Mà hợp chất ion có những tính chất chung sau:
+ Là chất rắn ở điều kiện thường
+ Thường có nhiệt độ nóng chảy và nhiệt độ sôi cao
+ Khi tan trong nước tạo ra dung dịch dẫn được điện
=> Ở điều kiện thường, potassium chloride là chất rắn

Nguyên tử K liên kết với nguyên tử Cl tạo thành phân tử potassium chloride. Khi phân tử potassium chloride tan trong nước tạo thành dung dịch có t/c nào dưới đây?
A. Dẫn điện
B. Không dẫn điện
C. Dễ bay hơi
D. Dễ cháy
- Là chất rắn ở điều kiện thường.
- Thường có nhiệt độ nóng chảy và nhiệt độ sôi cao.
- Khi tan trong nước tạo ra dung dịch dẫn được điện.

- Nguyên tử N nằm ở ô số 7, nhóm VA => Có 5 electron ở lớp ngoài cùng, cần 3 electron để đạt cấu hình khí hiếm
- Nguyên tử C nằm ở ô số 6, nhóm IVA => Có 4 electron ở lớp ngoài cùng, cần 4 electron để đạt cấu hình khí hiếm
- Nguyên tử O nằm ở ô số 8, nhóm VIA => Có 6 electron ở lớp ngoài cùng, cần 2 electron để đạt cấu hình khí hiếm
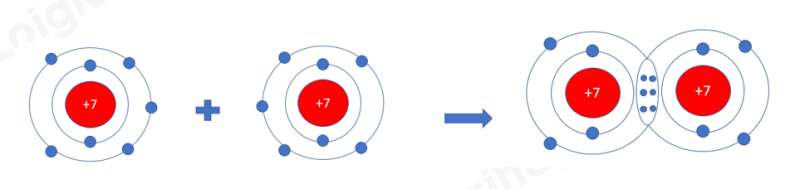
a) Xét phân tử Nitrogen: gồm 2 nguyên tử N
=> Liên kết cộng hóa trị, mỗi N góp 3 electron tạo thành 3 cặp electron dùng chung
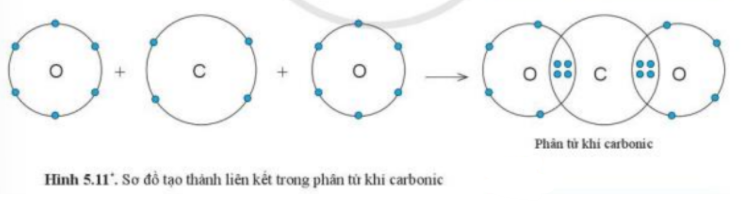
b) Xét phân tử Carbon dioxide: gồm 1 nguyên tử C và 2 nguyên tử O
=> Liên kết cộng hóa trị. Khi C kết hợp với O, nguyên tử C góp 4 electron, mỗi nguyên tử O góp 2 electron
=> Giữa nguyên tử C và nguyên tử O có 2 cặp electron dùng chung

Nguyên tử Nitrogen: Có `2` lớp electron và có `5` electron lớp ngoài cùng.
Nguyên tử Silicon: Có `3` lớp electron và có `4` electron lớp ngoài cùng.

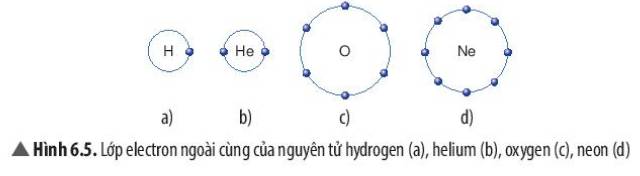
- Xét phân tử hydrogen: mỗi nguyên tử hydrogen có 2 electron lớp ngoài cùng
=> Giống cấu hình electron của nguyên tử khí hiếm Helium
- Xét phân tử Oxygen: mỗi nguyên tử Oxygen có 8 electron ở lớp ngoài cùng
=> Giống cấu hình electron của nguyên tử khí hiếm Neon

- Số electron dùng chung của nguyên tử H và O là 4
- Trong phân tử nước:
+ Nguyên tử O có 8 electron lớp ngoài cùng => Giống khí hiếm Ne
+ Nguyên tử H có 2 electron lớp ngoài cùng => Giống khí hiếm He




K cho đi 1e để nhận được cấu hình khí hiếm
Tham khảo