Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quặng đolômit có thành phần chính là CaCO3.MgCO3
Bảo toàn C: nCO2 = 0,4 = nCaCO3 + nMgCO3 ⇒ nCaCO3 = nMgCO3 = 0,2
mCaCO3.MgCO3 = 0,2.100 + 0,2.84 =36,8g
⇒ Độ tinh khiết =(36,8: 40).100% = 92%
Đáp án D.

Chọn đáp án D
Quặng đôlômit: M g C O 3 . C a C O 3 → t 0 CaO + MgO + 2 C O 2
0,2 ← 0,4 (mol)
Độ tinh khiết = 0 , 2 . 184 40 . 100% = 92%

\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
_______0,4<-----------------------0,4______(mol)
=> \(m_{CaCO_3}=0,4.100=40\left(g\right)\)
=> \(\%m_{CaCO_3}=\dfrac{40}{50}.100\%=80\%\)

Quặng đolômit có thành phần chính là CaCO3.MgCO3
Phần khối lượng giảm = mCO2 = 25 -14 =11g
⇒ nCO2 = 0,25; Bảo toàn C ⇒ nMgCO3 + nCaCO3 = 0,25 mol
⇒ nMgCO3 = nCaCO3 = 0,125
m CaCO3.MgCO3 = 0,125.100 + 0,125.84 = 23g
⇒ m tạp chất = 2g
⇒ %m tạp chất = (2 : 25).100% = 8%
Đáp án C.

Đáp án A
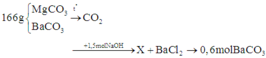
X + BaCl2 thu được kết tủa
Trong X chứa Na2CO3 và n N a 2 C O 3 = n B a C O 3 = 0,6
Vậy khi cho CO2 phản ứng với NaOH ta có phản ứng:
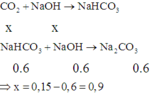
Gọi a và b lần lượt là số mol của MgCO3 và BaCO3 ta có:
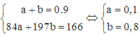

Đáp án C
Hướng dẫn giải:
Độ dinh dưỡng của phân kali được tính bằng %mK2O
Xét 100 gam phân có 55 gam K2O → nK2O= 55/ 94 (mol)
Bảo toàn nguyên tố K ta có: nKCl=2.nK2O= 2.55/94= 55/47 mol → mKCl= 55 × 74 , 5 47 =87,18 gam
→%mKCl= 87,18%
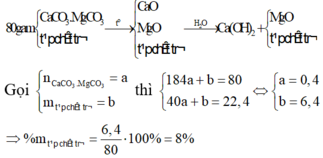

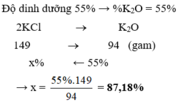
Quặng đôlomit có thành phần MgCO3 .CaCO3
CaCO3.MgCO3 \(\rightarrow\) CaO + MgO + 2CO2 ↑
0,2_________________________0,4
Thành phần phần trăm về khối lượng của CaCO .MgCO trong loại quặng là :
%CaCO3.MgCO3 =\(\frac{0,2.\left(100+84\right)}{40}.100\%=92\%\)
MgCO3.CACO3=>CO2
nCo2=0.4=>nCACO3.MgCO3=0.2=>m=36.8g=>%=36.8*100/40=92%