Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol KMnO4 và KClO3 trong hỗn hợp ban đầu lần lượt là x,y
158x + 122,5y= 48,2 (1)
Bảo toàn elcton toàn quá trình ta có
Mn+7+5e →Mn+2
x 5x
Cl+5 + 6e → Cl–1
y 6y
(về bản chất có 1 phần Cl+5 có 1 phần chuyển sang Cl0, nhưng Cl–1 lại nhường e tạo Cl0 vì vậy để đơn giản ta có thể coi tất cả Cl+5 tạo thành Cl–1)
2Cl–1→ Cl2 +2e
0,675 0,135
2O–2 → O2 + 4e
0,15 0,6
Áp dụng định luật bảo toàn e ta có 5x+6y=1,95 (2)
Từ 1 và 2 ta có hệ phương trình
Giải ta được x=0,15 và y=0,2
% mKMnO4 = 49,17 % và % mKClO3 =50,83%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Bảo toàn khối lượng
=> n O2 = (18,96 - 18,32)/32 = 0,02(mol)
n Cl2 = 12,544/22,4 = 0,56(mol)
n KMnO4 = 18,96/158 = 0,12(mol)
n KClO3 = a(mol)
Bảo toàn nguyên tố với Mn :
n MnCl2 =n KMnO4 = 0,12(mol)
Bảo toàn electron :
5n MnCl2 + 6n KClO3= 4n O2 + 2n Cl2
<=> 0,12.5 + 6a = 0,02.4 + 0,56.2
<=> a = 0,1
=> m = 0,1.122,5 = 12,25 gam

\(12,9g.hh\left\{{}\begin{matrix}Al:x\left(mol\right)\\Mg:y\left(mol\right)\end{matrix}\right.\underrightarrow{+Cl_2}Rắn.Y\left(37,45g\right)\underrightarrow{+HCl}H_2\left(64\%\right)\underrightarrow{+Fe_2O_3\left(50g\right)}Rắn\left(47,44g\right)\)
BTKL: \(m_X+m_{Cl_2}=m_Y\Rightarrow n_{Cl_2}=0,35\left(mol\right)\)
\(m_{Fe_2O_3}=m_{rắn}+m_{O\left(oxit\right)}\Rightarrow m_O=2,56\left(g\right)\\ \Rightarrow n_O=n_{H_2.pứ}=\dfrac{2,56}{16}=0,16\left(mol\right)\)
\(\Rightarrow n_{H_2.thoát.ra}=\dfrac{0,16}{64\%}.100\%=0,25\left(mol\right)\)
Bảo toàn mol e:
| Cho e | Nhận e |
| Mg - 2e --> \(Mg^{+2}\) | \(Cl_2^0+2e\) --> \(2Cl^-\) |
| x -> 2x | 0,35-> 0,7 |
| Al - 3e --> \(Al^{+3}\) | \(2H^++2e\) --> \(H_2\) |
| y -> 3y | 0,5<- 0,25 |
| \(N_e.cho=2x+3y\) | \(N_e.nhận=0,7+0,5=1,2\) |
\(\Rightarrow\left\{{}\begin{matrix}27x+24y=12,6\\2x+3y=1,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{3}{11}\\y=\dfrac{12}{55}\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%_{m_{Al}}=\dfrac{\dfrac{3}{11}.27.100\%}{12,6}=58,44\%\\\%_{m_{Mg}}=\dfrac{\dfrac{12}{55}.24.100\%}{12,6}=41,56\%\end{matrix}\right.\)

(a)- Khi cho E tác dụng với NaHCO3 sinh ra V lít khí (CO2) và muối natri của X => X là axit
- Ta thấy thể tích khí sinh ra khi cho E tác dụng với Na (khí H2) lớn hơn 0,5 lần thể tích khí khi cho E tác dụng với NaHCO3 (khí CO2) => Y là ancol
Vậy E gồm axit X, ancol Y và este Z (tạo bởi X, Y)
Giả sử V lít tương ứng với 1 (mol) khí
+ nCO2 = n-COOH = 1 (mol)
+ nH2 = 0,5n-COOH + 0,5n-OH => 0,75 = 0,5.1 + 0,5n-OH => n-OH = 0,5 (mol)
+ n hỗn hợp = 2nH2 = 1,5 mol => nX = nY = nZ = 1,5:3 = 0,5 mol
Số chức của axit X là: 1 : 0,5 = 2
Số chức của ancol Y là: 0,5 : 0,5 = 1
=> Este Z có 2 chức
* Đốt cháy muối natri của X:
Muối natri của X có dạng RO4Na2
Gọi số mol muối của X là x (mol)
BTNT Na: nNa2CO3 = n muối = x (mol)
BTNT O: 4n muối + 2nO2 = 2nCO2 + nH2O + 2nNa2CO3
=> 4x + 2nO2 = 0,03.2 + 0,02 + 3x => nO2 = 0,04 – 0,5x (mol)
BTKL: m muối + mO2 = mCO2 + mH2O + mNa2CO3
=> 1,62 + 32(0,04 - 0,5x) = 0,03.44 + 0,02.18 + 106x
=> x = 0,01 mol
=> M muối = 162 => R + 16.4 + 23.2 = 162 => R = 28 => CTPT của X là C4H6O4
* Đun nóng Y với H2SO4 đặc thu được Y1 có tỉ khối so với Y là 34/43 => phản ứng tách nước tạo anken
=> MY1 = MY – 18
=> dY1/Y = (MY-18)/MY = 34/43 => MY = 86 (C5H10O)
Mà khi đun Y1 với KMnO4/H2SO4 thu được Y2 duy nhất, không có khí thoát ra, Y2 có cấu tạo mạch thẳng và là điaxit nên Y1 có cấu tạo mạch vòng, chứa 1 liên kết đôi.
- Cấu tạo Y1:
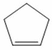
- Cấu tạo Y2: HOOC-(CH2)3-COOH
- Cấu tạo Y: 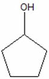
- Cấu tạo X:
HOOC-CH2-CH2-COOH hoặc HOOC-CH(CH3)-COOH
- Cấu tạo Z:
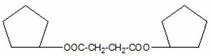
Hoặc
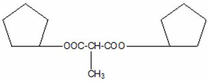
(b)Giả sử số mol mỗi chất trong ½ hỗn hợp G:
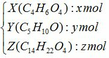
- Khối lượng của ½ hỗn hợp G:
118x + 86y + 254z = 7,8 (1)
- Đốt cháy phần 1 cần nO2 = 9,408 : 22,4 = 0,42 mol:
C4H6O4 + 3,5 O2 → 4CO2 + 3H2O
x 3,5x
C5H10O + 7O2 → 5CO2 + 5H2O
y 7y
C14H22O4 + 17,5O2 → 14CO2 + 11H2O
z 17,5z
Ta có: nO2 = 0,42 => 3,5x + 7y + 17,5z = 0,42 (2)
- Phần 2 tác dụng vừa đủ với nNaOH = 0,04.2 = 0,08 mol:
C2H4(COOH)2 + 2NaOH → C2H4(COONa)2 + 2H2O
x 2x x
C2H4(COOC5H9)2 + 2NaOH → C2H4(COONa)2 + 2C5H9OH
z 2z z 2z
nNaOH = 2nX + 2nZ => 2a + 2c = 0,08 (3)
Từ (1) (2) (3) ta có hệ phương trình:
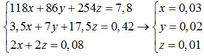
Sau phản ứng thu được:
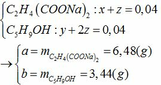

Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

\(n_{CaCO_3}=n_{MgCO_3}=a\left(mol\right)\\ CaCO_3-^{^{t^{^0}}}->CaO+CO_2\\ MgCO_3-^{^{t^{^0}}}->MgO+CO_2\\ CaO+H_2O->Ca\left(OH\right)_2\\ C:MgO\\ n_C=a=n_{MgCO_3}=\dfrac{20}{40}=0,5mol\\ x=0,5\left(100+84\right)=92\left(g\right)\\ V_{CO_2}=y=22,4.2a=22,4\left(L\right)\)
