Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CTTQankan:CnH2n+2
CTTQanken:CmH2m
\(n_{ankan}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow M_{ankan}=\frac{3}{0,1}=30\left(\frac{g}{mol}\right)\)
\(14n+2=30\Rightarrow n=2\)
Vậy ankan là C2H6
\(n_{hh}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(\Rightarrow n_{anken}=0,25-0,1=0,15\left(mol\right)\)
\(M_{anken}=\frac{6,3}{0,15}=42\left(\frac{g}{mol}\right)\)
\(14m=42\Rightarrow m=3\)
Vậy anken là C3H6

Ankan A có dạng CnH2n+2; anken B có dạng CmH2m.
Đốt A cho \(n_A=n_{H2O}-n_{CO2}\)
Đốt B cho \(n_{CO2}=n_{H2O}\)
Ta có:
\(n_{CO2}=\frac{1,792}{22,4}=0,08\left(mol\right)\)
\(n_{H2O}=\frac{1,62}{18}=0,09\left(mol\right)\)
\(\Rightarrow n_A=0,09-0,08=0,01\left(mol\right)\Rightarrow n_B=0,02\left(mol\right)\)
Dẫn X qua brom dư thì chỉ có B phản ứng nên khối lượng bình tăng là khối lượng của B.
\(\Rightarrow m_B=0,84\left(g\right)\Rightarrow M_B=14m=\frac{0,84}{0,02}=42\Rightarrow m=3\)
Vậy B là C3H6
\(\Rightarrow0,01.n+0,02.3=0,08\Rightarrow n=2\)
Vậy A là C2H6
\(\Rightarrow a=0,01.30+0,02.42=1,14\left(g\right)\)
Ankan A có dạng CnH2n+2; anken B có dạng CmH2m
Đốt A cho nA=nH2O−nCO2
Đốt B cho nCO2=nH2O
Ta có:nCO2=1,792\22,4=0,08 mol; nH2O=1,62\18=0,09 mol→nA=0,09−0,08=0,01 mol→nB=0,02 mol
Dẫn X qua brom dư thì chỉ có B phản ứng nên khối lượng bình tăng là khối lượng của B.
→mB=0,84 gam→MB=14m=0,84\0,02=42→m=3
Vậy B là C3H6C3H6
→0,01.n+0,02.3=0,08→n=2
Suy ra A là C2H6
→a=0,01.30+0,02.42=1,14 gam

a)
$C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O$
$2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O$
$C_2H_4 + Br_2 \to C_2H_4Br_2$
$C_2H_2 + 2Br_2 \to C_2H_2Br_4$
b)
n C2H4 = a(mol) ; n C2H2 = b(mol)
=> 28a + 26b = 2,96(1)
Mặt khác :
n B = 1,232/22,4 = 0,055(mol)
n Br2 = 13,6/160 = 0,085(mol)
Suy ra :
(a + b) / ( a + 2b) = 0,055/0,085 (2)
Từ (1)(2) suy ra a = 0,05 ; b = 0,06
Theo PTHH :
n CO2 = 2a + 2b = 0,22(mol) => m1 = 0,22.44 = 9,68(gam)
n CO2 = 2a + b = 0,16(mol) => m2 = 0,16.18 = 2,88(gam)

Bài 1.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_S=\dfrac{4,8}{32}=0,15mol\)
\(Fe+S\rightarrow\left(t^o\right)FeS\)
0,2 < 0,15 ( mol )
0,15 0,15 0,15 ( mol )
X gồm FeS và Fe(dư)
\(\left\{{}\begin{matrix}m_{FeS}=0,15.88=13,2g\\m_{Fe\left(dư\right)}=\left(0,2-0,15\right).56=2,8g\end{matrix}\right.\)
\(Fe+HCl\rightarrow FeCl_2+H_2\)
0,05 0,05 ( mol )
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
0,15 0,15 ( mol )
\(V_{hh}=V_{H_2}+V_{H_2S}=\left(0,05+0,15\right).22,4=4,48l\)
Bài 2.
\(n_{SO_2}=\dfrac{2,688}{22,4}=0,12mol\)
\(M+nH_2SO_4\left(đ\right)\rightarrow\left(t^o\right)\dfrac{1}{2}M_2\left(SO_4\right)_n+\dfrac{n}{2}SO_2+nH_2O\)
\(\dfrac{0,24}{n}\) \(0,12\) ( mol )
\(\rightarrow\dfrac{0,24M_M}{n}=7,68\)
\(\Leftrightarrow M_M=32n\)
Xét:
n=1 --> Lưu huỳnh ( loại )
n=2 --> Cu ( nhận )
n=3 --> Loại
Vậy kim loại đó là Cu
\(n_{NaOH}=2.0,5=1mol\)
\(T=\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{1}{0,12}=8,3\) --> Tạo ra muối Na2SO3
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
0,12 0,12 ( mol )
\(C_{M_{Na_2SO_3}}=\dfrac{0,12}{0,5}=0,24M\)

gọi nFe2O3=a(mol) nCuO=b(mol) Sau khi cho qua H2 dư=> nFe=2a n Cu=b
Áp dụng bảo toàn e: nSO2=(6a+2b)/2=3a+b(mol)
m tăng= 56. 2a+ 64b-(3a+b)32=7,2 (1)
m hh ban đầu= 160a + 80b= 24(2)
Từ (1) và (2) ta được a=0,05 b=0,2
=> mFe =2,8(g) mCu=12,8(g)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
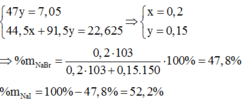

a.
CnH2n+H2Ni,to⟶CnH2n+2CmH2m−2+2H2Ni,to⟶CmH2m+2{CnH2n:xCmH2m−2:y→{x+y=100x+2y=160→{x=40y=60→%mol=%V{40%60%CnH2n+H2⟶Ni,toCnH2n+2CmH2m−2+2H2⟶Ni,toCmH2m+2{CnH2n:xCmH2m−2:y→{x+y=100x+2y=160→{x=40y=60→%mol=%V{40%60%
b.
Khi cho NaOH dư vào thu thêm được kết tủa nên dung dịch có muối Ca(HCO3)2.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,5 ← 0,15
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + 2H2O
0,1 ← 0,1
→ nCO2 = 0,1.2 + 0,5 = 0,7
Mặt khác: mdd giảm = mCaCO3 – mCO2 + mH2O
→ 9,12 = 50 – (44.0,7 + 18.nH2O) → nH2O = 0,56
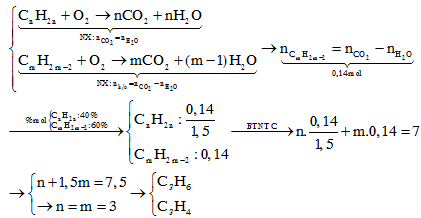

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)