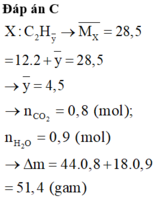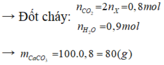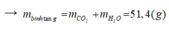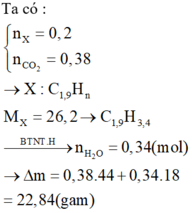Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
MX = 28,5g => nX = 0,4 mol
Vì trong X đều có các chất có số C = 2 => nC = 2nX = 0,8 mol
=> nH = mX– mC = 1,8 mol
=> Đốt cháy : nCO2 = 2nX = 0,8 mol ; nH2O = 0,9 mol
=> mCaCO3 = 100.0,8 = 80g
=> mbình tăng = mCO2 + mH2O = 51,4g

Đáp án C
MX = 14,25.2 = 28,5 => nX = 11,4: 28,5 = 0,4 mol
Ta thấy các chất trong X đều có 2 C => nC(X) = 2nX = 0,8 mol
Ta có: mX = mC + mH => mH = nH = 11,4 – 0,8.12 = 1,8
Bảo toàn nguyên tố: nCO2 = nC = 0,8 mol ; nH2O = ½ nH = ½. 1,8 = 0,9 mol
Khi sản phẩm cháy + bình Ca(OH)2 thì khối lượng bình tăng = khối lượng CO2 và H2O
=> mtăng = mCO2 + mH2O = 44.0,8 + 18.0,9 = 51,4g

Đáp án C
Xem X dạng có dạng CxH4 có M = 17 × 2 = 34 ⇒ x = 2,5 ⇒X là C2,5H4.
+ Đốt 0,1 mol C2,5H4 + O2 → 0,25 mol CO2 + 0,2 mol H2O.
⇒ mbình tăng = ∑mCO2 + ∑mH2O = 0,25 × 44 + 0,2 × 18 = 14,6 gam

Đáp án : A
X gồm C2H4 ; C3H4 ; C4H4 đều có 4 H
Có MX = 35,2g => nX = 0,2 mol
=> nH = 0,8 mol
=> nC = 0,52 mol
Khi đốt cháy : mbình tăng = 0,52.44 + 0,4.18 = 30,08g

Chọn D. X gồm C2H4 , CH4 , C3H4 , C4H4 . = 34g
→ mhh = 1,7 g
Do X gồm hidrocacbon có 4 H nên nH= 4nhh= 0,2 mol
→ nC = 0,125 mol → mtăng = mCO2 + mH2O = 44.nC +18. 0.5nH= 7,3 g