Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Vì thể tích H2 sinh ra khi cho X tác dụng với H2O < thể tích khí H2 sinh ra khi cho X tác dụng với KOH dư.
⇒ Khi X tác dụng với H2O Al vẫn còn dư.
Đặt số mol Al = a và nNa = b.
+ Pứ với H2O Al còn dư ⇒ nAl pứ = nNa = b.
⇒ Bảo toàn e: 3b + b = 0,2×2 = 0,4 (1).
+ Pứ với KOH dư ⇒ Tan hoàn toàn.
⇒ Bảo toàn e: 3a + b = 0,35×2 = 0,7 (2).
+ Giải hệ (1) và (2) ⇒ nAl = 0,2 và nNa = 0,1.
⇒ mX = 0,2×27 + 0,1×23 = 7,7 gam

Đáp án A
Vì thể tích H2 sinh ra khi cho X tác dụng với H2O < thể tích khí H2 sinh ra khi cho X tác dụng với KOH dư.
⇒ Khi X tác dụng với H2O Al vẫn còn dư.
Đặt số mol Al = a và nNa = b.
+ Pứ với H2O Al còn dư ⇒ nAl pứ = nNa = b.
⇒ Bảo toàn e: 3b + b = 0,2×2 = 0,4 (1).
+ Pứ với KOH dư ⇒ Tan hoàn toàn.
⇒ Bảo toàn e: 3a + b = 0,35×2 = 0,7 (2).
+ Giải hệ (1) và (2) ⇒ nAl = 0,2 và nNa = 0,1.
⇒ mX = 0,2×27 + 0,1×23 = 7,7 gam

HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.

Đáp án A
Xử Lý hỗn hợp khí X: 3 khí đó chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2 và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa N2 và N2O với MTrung bình = 36 = MTrung bình cộng của 2 khí.
⇒ nN2 = nN2O || Đặt nNO = a và nN2 = nN2O = b ta có hệ:
a + 2b = 0,04 || 30a + 28b + 44b = 1,32 ||⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận = 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là x và y ta có hệ:
(24+17×2)x + (27+17×3)y = 6,42 || 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol ⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ ⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2 = 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15 = 0,345 mol.
⇒ mDung dịch HNO3 = 0 , 345 × 63 × 100 24 = 90,5625 gam

Đáp án D
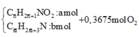
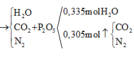
Bảo toàn C
![]()
Bảo toàn H:
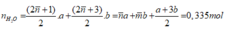
Dễ dàng tìm ra: b = 0,03 mol
Bảo toàn O: 2a + 0,3675.2 = 0,335 + 2 . ( 0,305−a+b2)
Thay b vào
→ a = 0,06 mol

Đáp án C
Đặt nAl = x; nNa = y ; nFe = z (mol)
P2 tác dụng với NaOH dư cho nhiều khí hơn P1
=>P1 Al chưa tan hết.
Ta có: mhh = 27x + 23y + 56z = 39,9
n khí P1 = y 2 + 3 y 2 = 0 , 2
n khí P2 = y 2 + 3 x 2 = 0 , 35
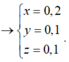
Vậy nếu t/d với dung dịch HCl thì ånkhí =
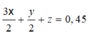
V = 0,45.22,4 = 10,08 lít
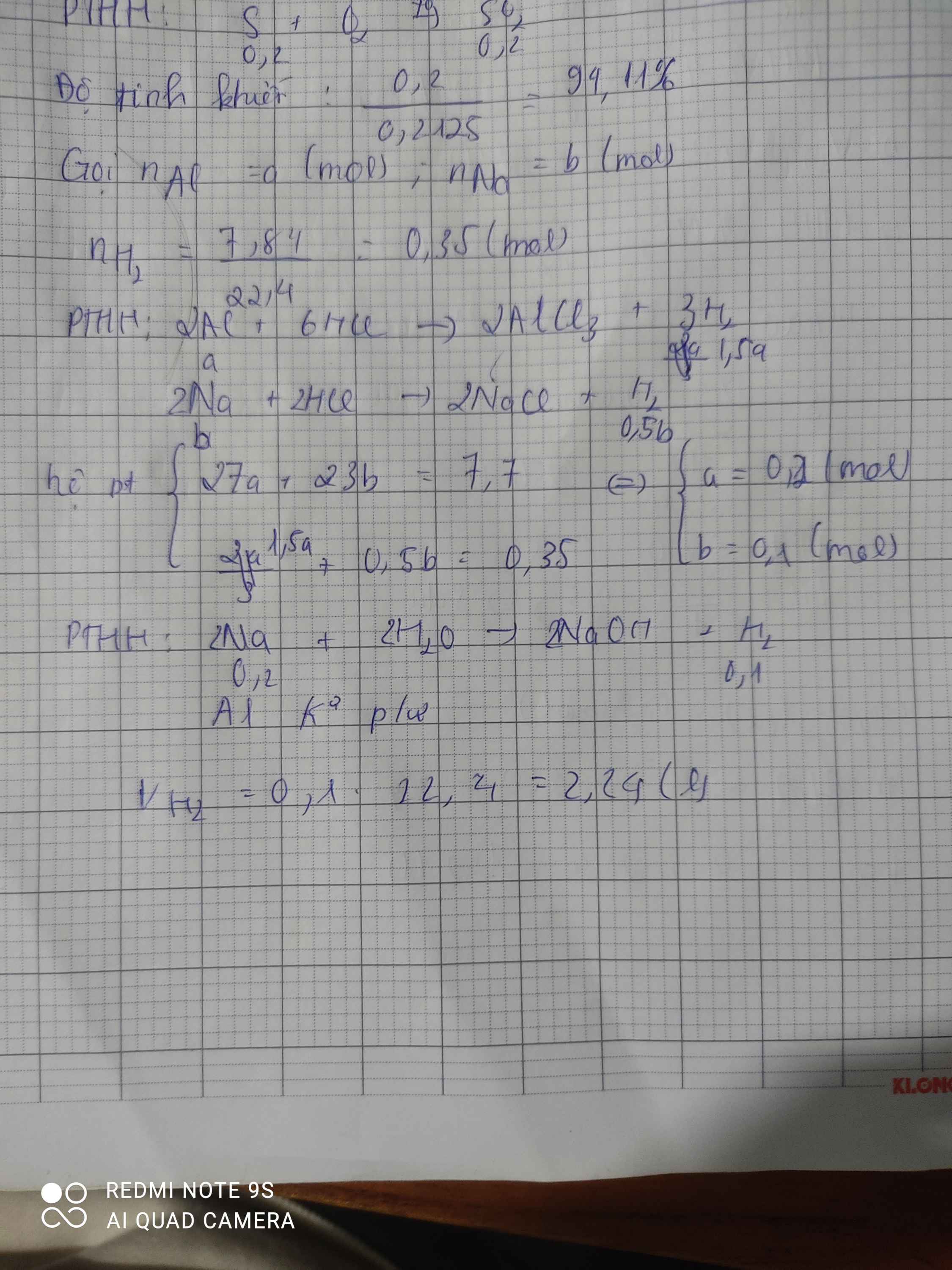
Đáp án A
Vì thể tích H2 sinh ra khi cho X tác dụng với H2O < thể tích khí H2 sinh ra khi cho X tác dụng với KOH dư.
⇒ Khi X tác dụng với H2O Al vẫn còn dư.
Đặt số mol Al = a và nNa = b.
+ Pứ với H2O Al còn dư
⇒ nAl pứ = nNa = b.
⇒ Bảo toàn e: 3b + b = 0,2×2 = 0,4 (1).
+ Pứ với KOH dư ⇒ Tan hoàn toàn.
⇒ Bảo toàn e: 3a + b = 0,35×2 = 0,7 (2).
+ Giải hệ (1) và (2)
⇒ nAl = 0,2 và nNa = 0,1.
⇒ mX = 0,2×27 + 0,1×23 = 7,7 gam