Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Coi hh chất rắn gồm M và O.
⇒ nO = 0,15.2 = 0,3 (mol)
Ta có: \(n_M=\dfrac{16,2}{M_M}\left(mol\right)\)
BT e, có: n.nM = 2nO + 2nSO2 + 6nS
\(\Rightarrow\dfrac{16,2n}{M_M}=1,8\Rightarrow M_M=9n\left(g/mol\right)\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
Vậy: M là Al.

Kim loại M có hóa trị n (n= 1,2,3)
nN2O = 6,72/22,4 = 0,3 mol => ne nhận = 0,3.8 = 2,4 mol
Áp dụng định luật bảo toàn electron => ne kim loại M nhường = 2,4 mol
Quá trình oxi hóa Quá trình khử
M → M+n + ne 2N+5 + 8e → N+12
\(\dfrac{2,4}{n}\) <----- 2,4 2,4<---- 0,3
=> nM = 2,4/n và phân tử khối M = \(21,6:\dfrac{2,4}{n}\) = 9n
=> n =3 và MM = 27 , kim loại M là nhôm (Al)

a)
M + 2HCl → MCl2 + H2
nH2 = \(\dfrac{3,584}{22,4}=\)0,16 mol => nM = 0,16 mol
<=> MM = \(\dfrac{3,84}{0,16}\)= 24 (g/mol) => M là magie (Mg).
b) 8Mg + 20HNO3 → 8Mg(NO3) + 2NO + N2 + 10H2O
Từ tỉ lệ phương trình , gọi số mol N2 là x => nNO = 2x mol
=> V(NO + N2) =3x.22,4 =1,344
<=> x =0,02
=> VN2 = 0,02.22,4 =0,448 lít , VNO= 0,04.22,4 = 0,896 lít

a) \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: 2M + 6HCl → 2MCl3 + 3H2
Mol: 0,02 0,06 0,02 0,03
\(M_M=\dfrac{0,54}{0,02}=27\left(g/mol\right)\)
⇒ M là nhôm (Al)
\(C\%_{ddHCl}=\dfrac{0,06.36,5.100\%}{500}=0,438\%\)
c) mdd sau pứ = 0,54 + 500 - 0,03.2 = 500,48 (g)
\(C\%_{ddAlCl_3}=\dfrac{0,02.133,5.100\%}{500,48}=0,53\%\)

a) Gọi kim loại cần tìm là R
\(n_R=\dfrac{7,56}{M_R}\left(mol\right)\)
PTHH: 2R + 2nHCl --> 2RCln + nH2
\(\dfrac{7,56}{M_R}\)------------>\(\dfrac{7,56}{M_R}\)
=> \(M_{RCl_n}=M_R+35,5n=\dfrac{37,38}{\dfrac{7,56}{M_R}}\)
=> \(M_R=9n\left(g/mol\right)\)
Xét n = 1 => MR = 9(Loại)
Xét n = 2 => MR = 18 (Loại)
Xét n = 3 => MR = 27(g/mol) => R là Al (Nhôm)
b)
\(n_{Al}=\dfrac{7,56}{27}=0,28\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,28-->0,84--->0,28--->0,42
=> \(V_{H_2}=0,42.22,4=9,408\left(l\right)\)
\(m_{HCl}=0,84.36,5=30,66\left(g\right)\)
=> \(m_{ddHCl}=\dfrac{30,66.100}{12}=255,5\left(g\right)\)
c) mdd sau pư = 7,56 + 255,5 - 0,42.2 = 262,22 (g)
=> \(C\%_{AlCl_3}=\dfrac{37,38}{262,22}.100\%=14,255\%\)

\(n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi số mol Al, Zn là a, b
=> 27a + 65b = 24,9
PTHH: 8Al + 30HNO3 --> 8Al(NO3)3 + 3N2O + 15H2O
______a------------------------------>0,375a
4Zn + 10HNO3 --> 4Zn(NO3)2 + N2O + 5H2O
b-------------------------------->0,25b
=> 0,375a + 0,25b = 0,15
=> a = 0,2 ; b = 0,3
=> \(\left\{{}\begin{matrix}\%Al=\dfrac{0,2.27}{24,9}.100\%=21,69\%\\\%Zn=\dfrac{0,3.65}{24,9}.100\%=78,31\%\end{matrix}\right.\)
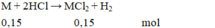
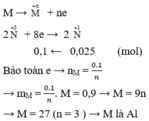
\(\text{Ta có }n_M=\dfrac{10,8}{M_M}\left(mol\right);n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:8M+30HNO_3\rightarrow8M\left(NO_3\right)_3+3N_2O+15H_2O\\ \Rightarrow n_M=\dfrac{8}{3}n_{N_2O}=0,4\left(mol\right)\\ \Rightarrow\dfrac{10,8}{M_M}=0,4\\ \Rightarrow M_M=27\)
Vậy M là nhôm (Al)