Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
nAl = 0,06 mol ; nHNO3 = 0,28 mol
=> Sau phản ứng : nAl3+ = 0,06 mol ; nH+ = 0,04 mol
Trộn A và B có kết tủa => Trong B còn OH- (HCl hết)
+) Giả sử phản ứng tạo kết tủa Al(OH)3 sau đó tan 1 phần
=> nAl(OH)3 = 4nAl3+ - nOH-
=> nOH- = 4.0,06 - 1,56/78=0,22 mol
=> nOH- (B) = 0,22 + 0,04trung hòa = 0,26 mol > 2nH2 = 2.0,125 = 0,25 mol
=> Phản ứng tạo kết tủa và Al3+ dư
=> nOH - = nH+ +3nAl(OH)3 = 0,1 mol
=> nH2 (do H+) = 0,125 - 1/2.0,1 = 0,075 mol
=> nHCl = 0,15 mol => a = 0,3 lít

Đáp án : B
nAl = 0,06 mol ; nHNO3 = 0,28 mol
Al + 4HNO3 à Al(NO3)3 + NO + 2H2O
=> nAl3+ = 0,06 mol ; nH+ dư = 0,04 mol
. Khi trộn X vào Y thì thu được kết tủa chính là Al(OH)3 => nAl(OH)3 = 0,02 mol
+) TH1 : Al3+ dư => nNaOH = 3nAl3+ pứ + nH+ = 3nAl(OH)3 + nH+ = 0,1 mol < 0,25 = nNa
Xét dung dịch X ta có : nNaOH = nNa ban đầu – nHCl => nHCl = 0,15 mol
=> CM(HCl) = 0,3M ( Có đáp án thỏa mãn )

Đáp án : A
nFe(OH)3 = 0,1 mol = nFe bđ => mO(X) = 4g
Qui X về 0,1 mol Fe và 0,25 mol O
Bảo toàn e : 3nFe = 2nO + 3nNO
=> nNO < 0 (Vô lý)
=> Fe3+ còn dư so với OH-
=> nOH- = nHNO3 dư + 3nFe(OH)3 => nHNO3 dư = 0,05 mol
=> nHNO3 pứ = 0,6 – 0,05 = 0,55 mol
Bảo toàn e : 3nFe = 2nO + 3nNO ; nHNO3 = 3nFe + nNO
Lại có : 56nFe + 16nO = 9,6g
=> nFe = 0,15 ; nO = 0,075 mol => nNO = 0,1 mol
=> V= 2,24 lit

Chọn B
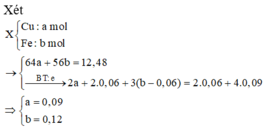
Khi cho X tác dụng với HNO3 thu được dung dịch T gồm Fe(NO3)2 (x); Fe(NO3)3 (y); Cu(NO3)2 (0,09).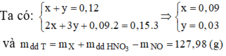
Vậy C% Fe(NO3)3 = 5,67%

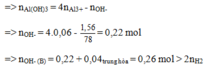

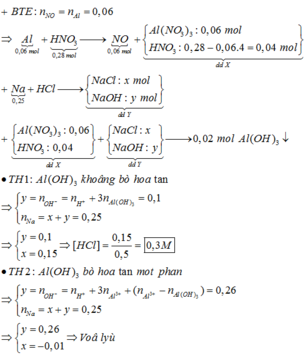


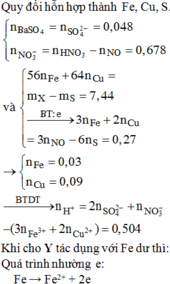

Chọn A.
Dung dịch A gồm Al(NO3)3 (0,06 mol) và HNO3 dư (0,04 mol)
Dung dịch B gồm M+, Cl- (0,5a mol) và OH- với
Khi cho A tác dụng với B thì kết tủa đang hình thành và chưa đạt cực đại