Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, nH2 = 0,6 (mol)
nHCl = 1,25 (mol)
Thấy : nHCl > 2nH2 => HCl dư
Gọi x là số mol của Mg , Al ( do nMg = nAl ) , y là số mol của Fe
PT : Mg + 2HCl → MgCl2 + H2↑
Mol : x------> 2x----------------->x
2Al + 6HCl → 2AlCl3 + 3H2↑
Mol : x --->3x------------------> 3/2x
Fe + 2HCl → FeCl2 + H2↑
Mol : y------>2y----------------> y
Ta có : 51x+ 56y = 15,8 và 5/2x + y = 0,6
=> x= 0,2 , y=0,1
=> %mMg = \(\frac{24.0,2}{15,8}.100\%\)= 30,38 %
%mAl = \(\frac{27.0,2}{15,8}.100\%\) = 34,18%
=> %mFe = 100 - 30,38 - 34,18 = 35,44%
b, mHCl pu = (0,6 + 0,4 + 0,2 ) .36,5 = 43,8 (g)
ĐLBTKL : mmuối = 15,8 + 43,8 - (0,6.2) = 58,4 (g)
c, Dung dịch A gồm 0,2mol AlCl3 , 0,2 mol MgCl2 , 0,1 mol FeCl2 và 0,05 mol HCl dư
CMHCl = \(\frac{0,05}{0,5}\)= 0,1M
CMFeCl2 = \(\frac{0,1}{0,5}\)= 0,2M
CMAlCl3 = CMMgCl2 = \(\frac{0,2}{0,5}\) = 0,4M

Đặt \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\Rightarrow65x+24y=8,9\left(1\right)\)
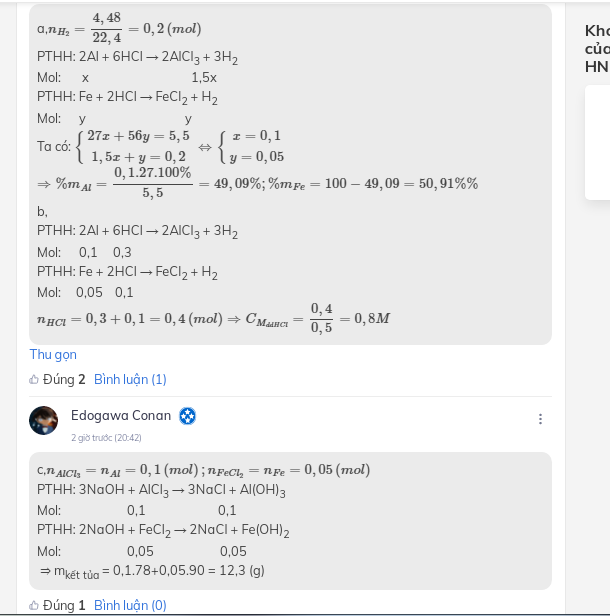
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ \Rightarrow x+y=0,2\left(2\right)\\ \left(1\right)\left(2\right)\Rightarrow\left\{{}\begin{matrix}65x+24y=8,9\\x+y=0,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\\ \Rightarrow\%_{Zn}=\dfrac{0,1\cdot65}{8,9}\cdot100\%\approx73\%\\ \Rightarrow\%_{Mg}=100\%-73\%=27\%\)
\(n_{HCl}=2x+2y=0,4\left(mol\right)\\ \Rightarrow m_{CT_{HCl}}=0,4\cdot36,5=14,6\left(g\right)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{14,6\cdot100\%}{14,6\%}=100\left(g\right)\)

a.
Số mol H2: nH2=2,24/22,4 =0,1 mol
Vì chỉ có Ca tác dụng với nước nên:
PT: Ca + 2H2O-->Ca(OH)2 + H2
0,1<--------------------------0,1 mol
Khối lượng Ca: mCa=0,1.40=4 g
mMg=8,8-4=4,8 g
b.
Trong hỗn hợp A:
nCa=4/40=0,1 mol
nMg=4,8/24=0,2 mol
PT:
Ca + 2HCl------->CaCl2 + H2
0,1-----------------------------0,1 mol
Mg + 2HCl-------->MgCl2 + H2
0,2--------------------------------0,2 mol
nH2=0,1 + 0,2=0,3 mol
Thể tích H2:
VH2=0,3.22,4=6,72 l

\(n_{HCl}=0.2\cdot2=0.4\left(mol\right)\)
\(BTKL:\)
\(m_{hh}+m_{HCl}=m_M+m_{H_2}\)
\(\Rightarrow m_M=8+0.4\cdot36.5-0.2\cdot2=22.2\left(g\right)\)
\(n_{Fe}=n_M=a\left(mol\right)\)
\(\Rightarrow a\left(56+M\right)=8\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+\dfrac{an}{2}=0.2\)
\(\Rightarrow a\left(1+\dfrac{n}{2}\right)=0.2\left(2\right)\)
\(\dfrac{\left(1\right)}{\left(2\right)}=\dfrac{a\left(56+M\right)}{a\left(1+\dfrac{n}{2}\right)}=\dfrac{8}{0.2}=40\)
\(\Rightarrow56+M=40\left(1+\dfrac{n}{2}\right)\)
\(\Rightarrow56+M=40+20n\)
\(\Rightarrow M-20n+16=0\)
\(BL:\)
\(n=2\Rightarrow M=24\)
\(M:Mg\)
\(\)
Gọi $n_{Mg} = n_{Al} = a(mol) ; n_{Fe} = b(mol)$
Ta có :
$24a + 27a + 56b = 15,8(1)$
$n_{HCl} > 2n_{H_2}$ nên HCl dư
Ta có :
$n_{H_2} = a + 1,5a + b = \dfrac{13,44}{22,4} = 0,6(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,1
$\%m_{Al} = \dfrac{0,2.27}{15,8}.100\% = 34,18\%$
$\%m_{Mg} = \dfrac{0,2.24}{15,8}.100\% = 30,38\%$
$\%m_{Fe} = 35,44\%$
$n_{HCl\ pư} = 2n_{H_2} = 1,2(mol)$
Bảo toàn khối lượng : $m_{muối} = 15,8 + 1,2.36,5 - 0,6.2 = 58,4(gam)$