Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có V1 < V2 => khi X tác dụng với H2O thì Al còn dư.
Giả sử số mol 3 kim loại là: x, y, z.
K + H2O → KOH + ½ H2↑
x → x 0,5x
Al + KOH + H2O → KAlO2 + 1,5H2↑
x ← x→ 1,5x
→ 0,5x + 1,5x = 0,2 → x = 0,1
X tác dụng với KOH: 0,1 . 0,5 + 1,5y = 0,35 => y = 0,2
Khi cho X tác dụng với H2O còn dư Al => Y chứa Al dư và Fe
nAl dư = nAl ban đầu – nAl phản ứng = 0,2 – 0,1 = 0,1mol
=> 0,1 . 1,5 + z = 0,4 => z = 0,25mol
=> m = 23,3g

Đáp án B
Phần chất rắn chưa tan là Al còn dư
Gọi n K = x mol
Cho hỗn hợp X vào nước, K phản ứng hết tạo KOH và Al phản ứng với KOH và còn dư => tính số mol theo KOH
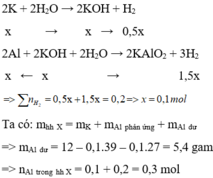
Cho hỗn hợp X tác dụng với dung dịch KOH dư => K phản ứng hết với H 2 O và Al phản ứng hết với KOH
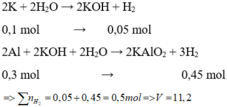

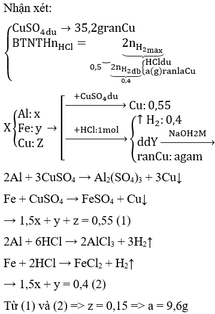
M g + 2 F e C l 3 → M g C l 2 + 2 F e C l 2 (1)
M g + 2 H C l → M g C l 2 + H 2 (2)
Từ phản ứng (2) ta có:
n M g = n H 2 = 2,688/22,4 = 0,12 mol
Dung dịch Y gồm 3 muối ⇒ M g C l 2 , F e C l 2 , F e C l 3 ⇒ F e C l 3 sau phản ứng (1) còn dư.
⇒ n F e C l 3 (1) = 2.nMg = 2.0,12 = 0,24g
F e + 2 F e C l 3 → 3 F e C l 2 (3)
⇒ n F e C l 3 (3) = 2 n F e = 0,04 mol
⇒ n F e C l 3 b d = n F e C l 3 ( 3 ) + n F e C l 3 ( 1 )
= 0,04+0,24 = 0,28g
⇒ m X = 0,12.24 + 0,28.(56+35,5.3) = 48,3g
⇒ Chọn C.