
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi công thức hoá học của ôxit sắt cần tìm là: FexOy
- Theo đề bài ra ta có: 56x / 56x + 16y = 70%
<=> 5600x = 3920x + 1120y
<=> 1680x = 1120y
<=> x / y = 1120 / 1680
<=> x / y = 2 / 3
=> Công thức hoá học của ôxit sắt cần tìm là: Fe2O3


a) Ta có: \(M_{XCO_3}=4\cdot25=100\) \(\Rightarrow M_X=100-12-16\cdot3=40\left(đvC\right)\)
\(\Rightarrow\) X là Canxi (Ca)
b) \(\%O=\dfrac{16\cdot3}{100}\cdot100\%=48\%\)
Bài 3:
a) M(XCO3)=25. M(He)= 25.4=100(đ.v.C)
Mặt khác: M(XCO3)=M(X)+ 60
=> M(X)+60=100
<=>M(X)=40(đ.v.C)
=> X là Canxi (Ca=40)
b) %mO=[(3.16)/100].100=48%

PTK(hợp chất)= 3:17,647%= 17(đ.v.C)
Mặt khác: PTK(hc)=NTK(X)+3
<=>17=NTK(X)+3
<=>NTK(X)=14(đ.v.C)
Vậy X là nito (N)
b) PTK(hc)=17(đ.v.C)
Anh Đạt đẹp trai chúc em học tốt!

Trong nguyên tử có số electrong bằng số proton hay p=e
2Z+N=28 và số hạt notron N chiếm 35% nên N=35%*28=9.8
Thay vào 2Z+N=28 ta được:
2Z+9.8=28
2Z=18.2
Z =9.1
Vậy số electron là 9.1
Trong đó Z vừa là electron vừa là proton, N là notron



$4Al+3O_2\xrightarrow{t^o}2Al_2O_3$
$n_{O_2}=\dfrac{V}{22,4}=\dfrac{6,72}{22,4}=0,3(mol)$
Theo PT: $n_{Al}=\dfrac{4}{3}n_{O_2}=0,4(mol)$
$\Rightarrow m_{Al}=n.M=0,4.27=10,8(g)$

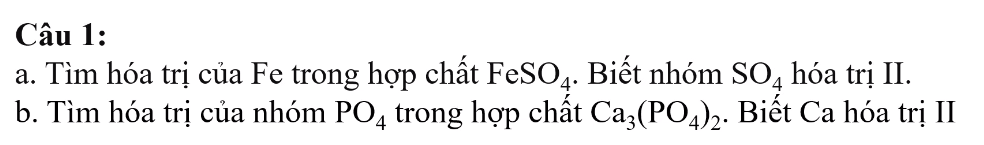



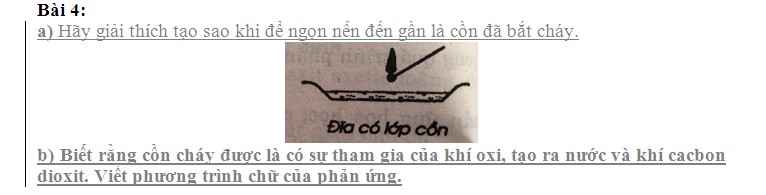 mấy anh chị giải chi tiết giùm em,em cần lời giải chi tiết ạ em xin cảm ơn
mấy anh chị giải chi tiết giùm em,em cần lời giải chi tiết ạ em xin cảm ơn
a)
$n_{Nito} = \dfrac{6,02.10^{23}}{6,02.10^{23}} = 1(mol)$
$m_{Nito} = 1.14 = 14(gam)$
b)
$n_{Cl} = \dfrac{6,02.10^{23}}{6,02.10^{23}} = 1(mol)$
$m_{Cl} = 1.35,5 = 35,5(gam)$
c)
$n_{H_2O} = \dfrac{6,02.10^{23}}{6,02.10^{23}} = 1(mol)$
$m_{H_2O} = 1.18 = 18(gam)$
a) \(n_{N_2}=\dfrac{6,02.10^{23}}{6,02.10^{23}}=1\left(mol\right)\)
=> \(m_{N_2}=1.28=28\left(g\right)\)
b) \(n_{Cl_2}=\dfrac{6,02.10^{23}}{6,02.10^{23}}=1\left(mol\right)\)
=> \(m_{Cl_2}=1.35,5.2=71\left(g\right)\)
c) \(n_{H_2O}=\dfrac{6,02.10^{23}}{6,02.10^{23}}=1\left(mol\right)\)
=> \(m_{H_2O}=1.18=18\left(g\right)\)
d) \(n_{CaCO_3}=\dfrac{6,02.10^{23}}{6,02.10^{23}}=1\left(mol\right)\)
=> \(m_{CaCO_3}=1.100=100\left(g\right)\)