Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Dung dịch X có chứa Cu2+ (x mol), H+ (y mol)![]()
Khối lượng thanh sắt giảm![]()
Khối lượng dung dịch giảm![]()
Từ (1), (2), (3) suy ra: a = 0,5

Chọn C.
Khí thoát ra tại anot gồm Cl2 (0,1 mol) và O2 (a mol).
![]() => mdd giảm = 64.(0,1 + 2a) + 71.0,1 + 32a = 21,5 Þ a = 0,05.
=> mdd giảm = 64.(0,1 + 2a) + 71.0,1 + 32a = 21,5 Þ a = 0,05.
Dung dịch X gồm NaNO3, HNO3 (4a = 0,2 mol) và Cu(NO3)2 dư (x – 0,2 mol).
Khi cho Fe vào dung dịch X thì:
3Fe + 8HNO3 ® 3Fe(NO3)2 + 2NO + 4H2O , Dmgiảm (1) = mFe ![]()
Fe + Cu(NO3)2 ® Fe(NO3)2 + Cu (2) , Dmtăng (2) = (64 – 56).(x – 0,2) = 8x – 1,6 (g)
Theo đề: 4,2 – (8x – 1,6) = 1,8 Þ x = 0,5.

Đáp án : D
Khi nhúng thanh sắt vào X thì tạo khí NO => có H+
Các quá trình có thể xảy ra :
Catot :
Cu2+ + 2e -> Cu
2H2O + 2e -> 2OH- + H2
Anot :
2Cl- -> Cl2 + 2e
2H2O -> 4H+ + O2 + 4e
+) TH1 : Cu2+ còn dư ; catot chưa điện phân nước
Gọi nH+ tạo ra = a mol => nO2 = 0,25a mol
=> ne = 2nCu2+ pứ = nCl- + nH+ => nCu2+ pứ = 0,1 + 0,5a (mol)
=> mgiảm = 64.(0,1 + 0,5a) + 32.0,25a + 0,1.71 = 21,5g
=> a = 0,2 mol
Số mol Cu2+ còn dư là (x – 0,2) mol
Vì nH+ = 0,2 < ½ nNO3- => H+ hết và chỉ phản ứng đến Fe2+ (Fe dư)
=> mthanh giảm = mFe pứ - mCu tạo ra
=> 2,6 = 56.(0,2.3/8 + x – 0,2) – 64.(x – 0,2)
=> x = 0,4 (Có đáp án thỏa mãn)

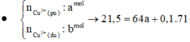
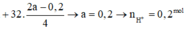

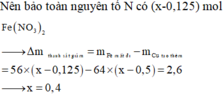




Đáp án C