
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

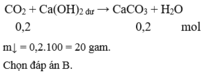

Đáp án C.
Số mol CO2 là: 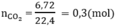
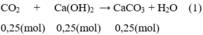
Theo pt (1): nCO2 = nCa(OH)2 = 0,25 mol
nCO2 (dư ) = 0,3 – 0,25 = 0,05 (mol)
Xảy ra phản ứng:
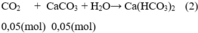
Theo pt(2): nCaCO3 pư = nCO2 = 0,05 mol
Như vậy CaCO3 không bị hòa tan là: 0,25 – 0,05 = 0,2(mol)
Khối lượng kết tủa thu được là m = 0,2. 100 = 20(g)

\(Ca^{2+} + CO_3^{2-} \to CaCO_3\\ CaCO_3 \xrightarrow{t^o} CaO + CO_2\\ n_{Ca^{2+}} = n_{CaO} = \dfrac{0,28}{56}=0,005(mol)\\ \text{Trong 10 ml dung dịch có chứa 0,005 mol ion}\ Ca^{2+}\\ \text{Vậy trong 1 lít(1000ml) dung dịch có chứa 0,005.100 = 0,5 mol ion}\ Ca^{2+}\\ m_{Ca^{2+}} = 0,5.40 = 20(gam)\)
Đáp án B

Đáp án A
Có
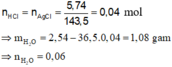
Khí thoát ra khỏi bình là CO2.
CO2 + 0,1 mol Ca(OH)2 → CaCO3 + dung dịch
Dung dịch thu được + Ba(OH)2 dư → BaCO3
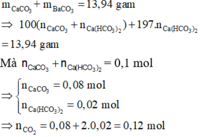
Áp dụng định luật bảo toàn khối lượng có:
mO(X) = 4,3 – 12.0,12 – 1.(2.0,06 + 0,04) – 35,5.0,04 = 1,28 gam
nO(X) = 0,08 mol
nC : nH : nO : nCl = 0,12 : 0,16 : 0,08 : 0,04 = 3:4:2:1
X có dạng C3nH4nO2nCln 107,5n < 230 n < 2,13 mà tổng số nguyên tử H và Cl phải là số chẵn n = 2
Trong phân tử X chứa 4 nguyên tử O