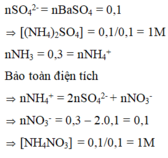Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Ba2++ SO42- →BaSO4
0,1 ← 23,3/233
NH4++ OH- →NH3+ H2O
0,3← 0,3
Theo ĐLBT ĐT thì: nNO3(-)=0,1 mol
Vậy dung dịch X có 0,1 mol (NH4)2SO4 và 0,1 mol NH4NO3
Suy ra nồng độ mol (NH4)2SO4 1M và NH4NO3 1M

Đáp án A
Gọi công thức TB của hai muối cacbonat là: M ¯ C O 3
M ¯ C O 3 → t 0 M O + C O 2 ( 1 )
Chất rắn Y ( M ¯ C O 3 ; M ¯ O )
n C O 2 ( 1 ) = 3 , 36 22 , 4 = 0 , 15 m o l
Y tác dụng với dung dịch HCl dư
M ¯ C O 3 + 2 H C l → t 0 M ¯ C l 2 + C O 2 + H 2 O ( 2 ) M ¯ O + H C l → t 0 M ¯ C l 2 + H 2 O ( 3 ) C O 2 + B a ( O H ) 2 → B a C O 3 + H 2 O ( 4 ) 2 C O 2 + B a ( O H ) 2 → B a ( H C O 3 ) 2 ( 5 ) B a ( H C O 3 ) 2 → t 0 B a C O 3 + C O 2 + H 2 O ( 6 ) n B a C O 3 ( 4 ) = 9 , 85 197 = 0 , 05 m o l n B a C O 3 ( 6 ) = 9 , 85 197 = 0 , 05 m o l
Theo PT (4,5,6): n C O 2 ( 3 ) = 0 , 15 m o l
Theo PT (1,2):
n M ¯ C O 3 = n C O 2 ( 2 ) + n C O 2 ( 1 ) = 0 , 15 + 0 , 15 = 0 , 3 m o l
Muối khan là: M ¯ C l 2
M ¯ C O 3 → M ¯ C l 2 M ¯ + 60 M ¯ + 71
0,3 mol muối cacbonat pư tạo 0,3 mol muối clorua tăng 3,3(g).
Khối lượng muối cacbonat ban đầu là: 38.15-3,3= 34,85(g)
Giá trị của m = 34,85(g)

Đáp án B
Hướng dẫn giải:
2NH4NO3 + Ba(OH)2 → Ba(NO3)2+ 2NH3↑+ 2H2O
2(NH4)3PO4 + 3Ba(OH)2 → Ba3(PO4)2+ 6NH3↑+6 H2O
Đặt nNH4NO3= x mol; n(NH4)3PO4= y mol → 80x + 149 y= 37,8 gam
Ta có nNH3= x + 3y = 15,68/ 22,4 mol
Giải hệ trên ta có x= 0,1 và y= 0,2 mol
→%m(NH4)3PO4= 0,2.149.100%/37,8= 78,84%

Đáp án C
Gọi số mol mỗi ion NH4+, K+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = 0,3 mol
mkết tủa= mBaCO3+ mBaSO4= 197z+233t= 43 suy ra t= 0,1 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol= 0,1
Định luật bảo toàn điện tích: x+y=2z+ 2t suy ra y= 0,1 mol
mmuối= (18x+ 39y+60z+96t).2= 49,8 gam

Đáp án D
nNH4+ = nNH3 = 0,02
Nếu cho dung dịch A tác dụng với dung dịch H2SO4 loãng, dư thì thu được 0,224 lít khí (đktc) ⇒ nCO32- = nCO2 = 0,01
mBaCO3 + mBaSO4 = 4,3 ⇒ nSO42- = 0,01
⇒ nNa+ = 0,02 ⇒ m = m Na+ + m NH4+ + m CO32- + m SO42- = 2,38g

nBaSO4 = 0,1 ; nNH3 = 0,3
Ba2+ + SO42- → BaSO4
0,1 ← 0,1 (mol)
NH4+ + OH- → NH3 + H2O
0,3 0,3 (mol)
Bảo toàn ion có nNO3- = 0,1
⇒ n(NH4)2SO4 = 0,1 ; nNH4NO3 = 0,1
⇒ Nồng độ mol/lít của (NH4)2SO4 và NH4NO3 lần lượt là 1M và 1M
Đáp án B.

Đáp án A
Gọi số mol Al3+, NH4+, SO42- trong 100 ml dung dịch Y lần lượt là x, y, z mol
-Phần 1:
Al3++ 3NH3+ 3H2O→ Al(OH)3+ 3NH4+
x/5 x/5 = 2.10-3 suy ra x = 0,01 mol
-Phần 2:
Ba2++ SO42-→ BaSO4
z/5 mol z/5 mol = 0,932/233 = 4.10-3 mol nên z = 0,02 mol
ĐLBT ĐT suy ra y = 0,01 mol suy ra nH2O = 0,12 mol
Suy ra CT là Al.NH4.(SO4)2.12H2O