
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(n_{KClO_3}=\dfrac{5,5125}{122,5}=0,045\left(mol\right)\\ 2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\uparrow\\ n_{O_2}=\dfrac{3}{2}.0,045=0,0675\left(mol\right)\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{CuO}=2.0,0675=0,135\left(mol\right)\\ m_{r\text{ắn}}=m_{CuO}=0,135.80=10,8\left(g\right)\)


a. \(Mg+2HCl\rightarrow MgCl_2+H_2\)
tỉ lệ 1 : 2 : 1 : 1
b. áp dụng định luật bảo toàn khối lượng, ta có:
\(m_{Mg}+m_{HCl}=m_{MgCl_2}+m_{H_2}\)
\(m_{MgCl_2}=m_{Mg}+m_{HCl}-m_{H_2}\)
\(=30+9,8-12,2=27,6\left(kg\right)\)
vậy khối lượng muối magie clorua tạo thành sau phản ứng là \(27,6kg\)

Gọi kim loại cần tìm là R (II)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_R=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow56a+M_R.b=8\left(g\right)\)
\(n_{HCl}=0,2.2=0,4\left(mol\right)\)
PTHH:
Fe + 2HCl --->FeCl2 + H2
a---->2a
R + 2HCl ---> RCl2 + H2
b---->2b
Theo pthh: \(n_{hhkl}=n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, Lập được hệ pt: \(\left\{{}\begin{matrix}56a+M_R.b=8\\2a+2b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\\M_R=24\left(\dfrac{g}{mol}\right)\end{matrix}\right.\)
=> R là Mg
c, \(\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_{Mg}=0,1\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Mg}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
Quy hết kim loại R (II) và Fe về M (II):
\(n_{HCl}=0,2.2=0,4\left(mol\right)\)
PTHH: M + 2HCl ---> MCl2 + H2↑
0,2<-0,4------->0,2---->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
\(b,M_M=\dfrac{8}{0,2}=40\left(\dfrac{g}{mol}\right)\\ \rightarrow M_R=2.40-56=24\left(\dfrac{g}{mol}\right)\)
=> R là Mg
c, Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
a---->2a--------->a
Mg + 2HCl ---> MgCl2 + H2
b---->2b-------->b
=> hệ pt \(\left\{{}\begin{matrix}56a+24b=8\\2a+2b=0,4\end{matrix}\right.\Leftrightarrow a=b=0,1\left(mol\right)\left(TM\right)\)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Mg}=0,1.24=2,4\left(g\right)\end{matrix}\right.\)
d, \(\left\{{}\begin{matrix}C_{M\left(FeCl_2\right)}=\dfrac{0,1}{0,2}=0,5M\\C_{M\left(MgCl_2\right)}=\dfrac{0,1}{0,2}=0,5M\end{matrix}\right.\)

bạn bấm máy tính hoặc giải hệ:
\(\left\{{}\begin{matrix}27x+56y=11\\1,5x+y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}27x+56y=11\\84x+56y=22,4\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}57x=11,4\\27x+56y=11\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\27.0,2+56y=11\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)

a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right);n_{H_2SO_4}=0,1.0,5=0,05\left(mol\right)\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Theo đề:0,2......0,05
Lập tỉ lệ: \(\dfrac{0,2}{2}>\dfrac{0,05}{3}\)=> Al dư, H2SO4 hết
=> \(V_{H_2}=0,05.22,4=1,12\left(l\right)\)
=> Chọn C
b) \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{H_2SO_4}=\dfrac{0,05}{3}=\dfrac{1}{60}\left(mol\right)\)
=> \(C_{M\left(Al_2\left(SO_4\right)_3\right)}=\dfrac{1}{\dfrac{60}{0,1}}==0,17M\)
=> Chọn A

Fe3O4 + 3H2 -> 3Fe + 4H2O
232 3\(\times\)56 (M)
\(mFe3O4=1.5\times80\%=1.2\) tấn
\(mFe=\dfrac{1.2\times3\times56}{232}=0.87\) tấn
Chọn D

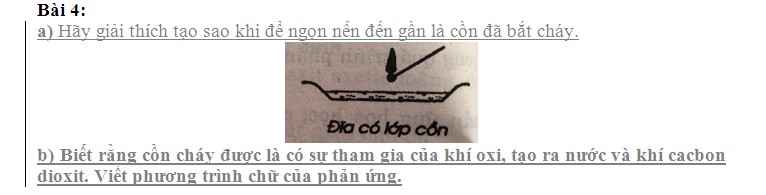 mấy anh chị giải chi tiết giùm em,em cần lời giải chi tiết ạ em xin cảm ơn
mấy anh chị giải chi tiết giùm em,em cần lời giải chi tiết ạ em xin cảm ơn
 m giải chi tiết ạ
m giải chi tiết ạ


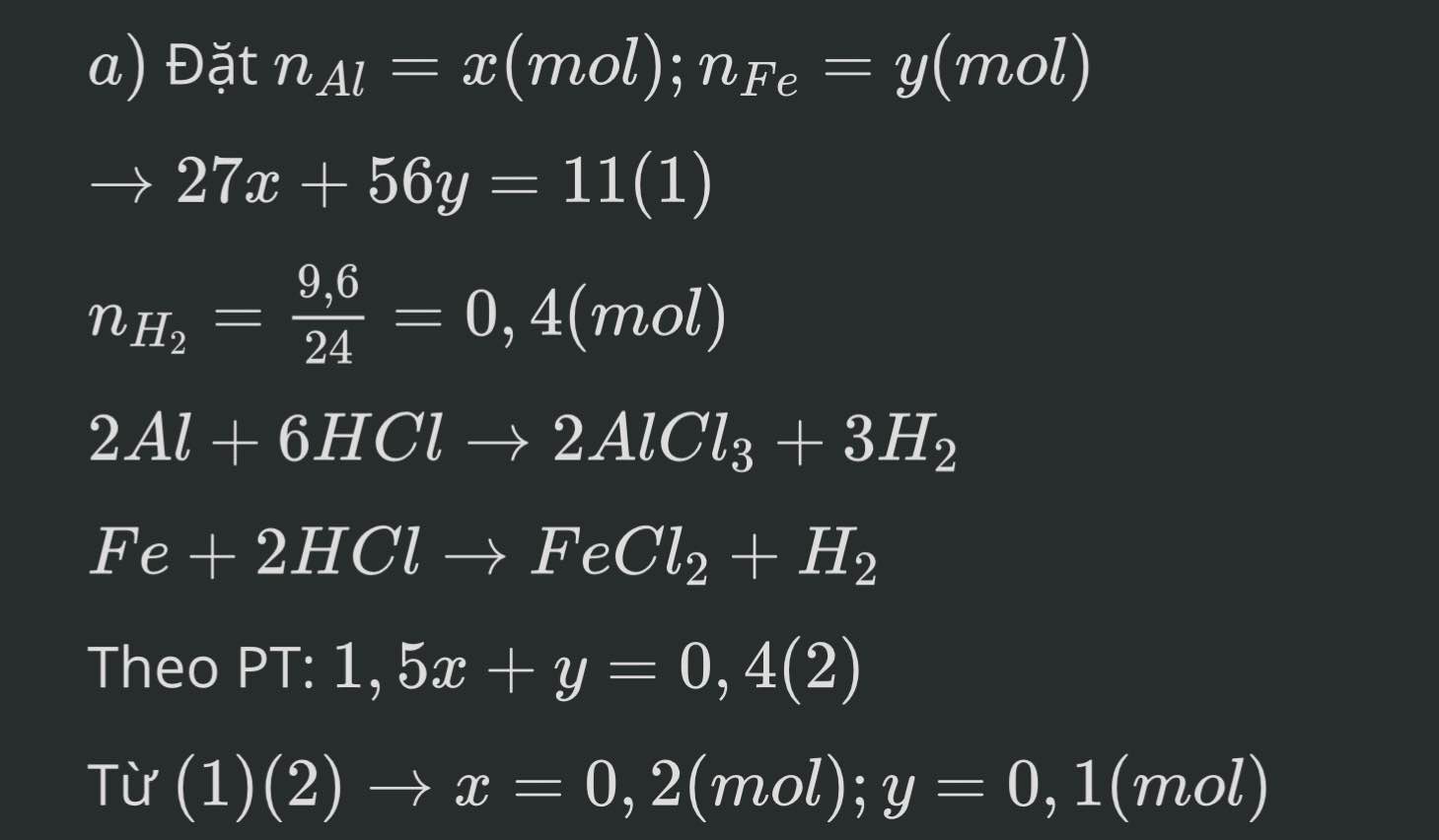


\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\ pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,4 0,4 0,4
\(V_{H_2}=0,4.22,4=8,96l\\ m_{FeCl_2}=0,4.127=50,8g\\ n_{Fe_2O_3}=\dfrac{14}{160}=0,0875\left(mol\right)\\ pthh:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(LTL:\dfrac{0,0875}{1}< \dfrac{0,4}{3}\)
=> H2 dư
\(n_{H_2\left(p\text{ư}\right)}=3n_{Fe_2O_3}=0,2625\left(mol\right)\\ m_{H_2\left(d\right)}=\left(0,4-0,2625\right).2=0,275g\\ n_{Fe}=2n_{Fe_2O_3}=0,175\left(mol\right)\\ m_{Fe}=0,175.56=9,8g\)