Mn giải hộ mik bài này vs ạ, theo kiểu biện luận Cho hỗn hợp Y gồm 2,8g Fe và 0,81 Al vào 200ml dung dịch C chứa AgNO3 và Cu(NO3)2. Khi phản ứng kết thúc thu được dung dịch D và 8,12g chất rắn E gồm 3 kim loại. Cho rắn E tác dụng với HCl dư thì thu được 0,672l H2 (đktc). Tính Cm của AgNO3 và Cu(NO3)2 trong dung dịch C.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A.
Vì phản ứng giữa Al và AgNO3 xảy ra trước nên kim loại sau phản ứng phải có Ag, kế đến là CuSO4 có phản ứng tạo thành Cu. Theo giả thiết, có ba kim loại → kim loại thứ ba là Fe còn dư.
Ta có: nFe = 2,8/5,6 = 0,05 (mol)
nAl = 0,81/27 = 0,03 (mol)
và = 0,672/22,4 = 0,03 (mol)
Phản ứng: Fedư + 2HCl → FeCl2 + H2
(mol) 0,03 0,03
→ Số mol Fe phản ứng với muối: 0,05 – 0,03 = 0,02 (mol)
2Al + 3Cu2+ → 2Al3+ + 3Cu
Fe + 2Ag+ → Fe2+ + 2Ag
Fe + Cu2+ → Fe2+ + Cu
Ta có sự trao đổi electron như sau:
Al → Al3+ + 3e Fe → Fe2+ + 2e
0,03 0,09 (mol) 0,02 0,04 (mol)
Ag+ + 1e → Ag Cu2+ + 2e → Cu
x x x (mol) y 2y y (mol)
→ x + 2y = 0,09 + 0,04 = 0,13 (1) ; 108x + 64y + 56.0,03 = 8,12 (2)
Giải hệ phương trình (1) và (2), ta được x = 0,03; y = 0,05.
Vậy:


Chọn đáp án A
![]()
⇒ E gồm 3 kim loại thì đó là Ag, Cu và Fe dư ⇒ nFe dư = nH2 = 0,03 mol
Đặt n A g + = x mol; n C u 2 + = y mol ||→ mE = 8,12 gam = 108x + 64y + 0,03 × 56
![]()
![]()
Giải hệ có: x = 0,03 mol; y = 0,05 mol
![]()

Đáp án A
Vì T chứa 3 kim loại nên T chứa Cu, Ag và Fe dư (Al phản ứng trước Fe).
Khi đó Al, Cu2+ và Ag+ phản ứng hết.
Khi cho T phản ứng với HCl dư, chỉ có Fe phản ứng
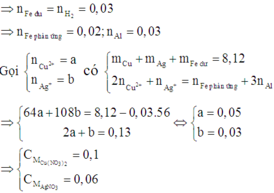

Đáp án B
M tác dụng Fe(NO3)3 và AgNO3 thu được 2 kim loại M và Ag và 2 muối. Pt như sau:
M + Fe3+ → M2+ + Fe2+. Ta có cặp điện cực M2+/M đứng trước Fe3+/Fe2+.
M + Ag+ → M2+ + Ag. Ta có cặp điện cực M2+/M đứng trước Ag+/Ag
Vì không tạo ra kim loại Fe nên M có tính khử yếu hơn Fe
Sắp xếp các cặp điện cực theo dãy điện hóa
Fe2+/Fe ; M2+/M ; Fe3+/Fe2+ ; Ag+/Ag.
Tính khử theo thứ tự: Fe > M > Fe2+ > Ag
Tính oxi hóa theo thứ tự: Ag+ > Fe3+ > M2+ > Fe2+

Đáp án D
Vì dung dịch C đã mất màu hoàn toàn nên cả Ag+ và Cu2+ đều phản ứng hết.
Mà B không tan trong HCl nên B chỉ chứa Ag và Cu. Do đó cả Al và Fe đều phản ứng hết.
Suy ra cho X vào A thì cả 4 chất đều phản ứng vừa đủ.
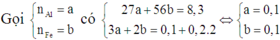
Vì dung dịch E đã nhạt màu nên Ag+ đã phản ứng hết và Cu2+ đã phản ứng một phần.
Do đó D chứa Ag và Cu.
Dung dịch E chứa Al3+, Fe2+ và Cu2+ dư. Khi đó E chứa Fe(OH)2 và Cu(OH)2
Suy ra F chứa Fe2O3 và CuO
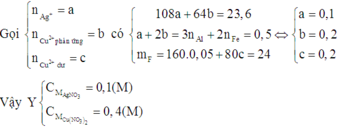
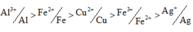
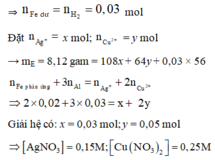

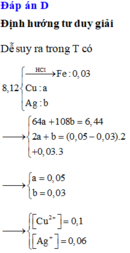
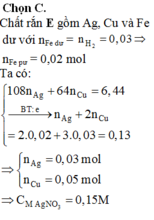
Ta có: \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(n_{Al}=\dfrac{0,81}{27}=0,03\left(mol\right)\)
- E gồm: Ag, Cu và Fe dư.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{Fe\left(dư\right)}=n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\) ⇒ nFe pư = 0,05 - 0,03 = 0,02 (mol)
⇒ mAg + mCu = 8,12 - 0,03.56 = 6,44 (g)
Gọi: \(\left\{{}\begin{matrix}n_{AgNO_3}=x\left(mol\right)\\n_{Cu\left(NO_3\right)_2}=y\left(mol\right)\end{matrix}\right.\)
BTNT Ag: nAg = nAgNO3 = x (mol)
BTNT Cu: nCu = nCu(NO3)2 = y (mol)
⇒ 108x + 64y = 6,44 (1)
Theo ĐLBT e, có: 2nFe pư + 3nAl = nAg+ + 2nCu2+ ⇒ nAg + 2nCu = 0,13 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,03\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{AgNO_3}}=\dfrac{0,03}{0,2}=0,15\left(M\right)\\C_{M_{Cu\left(NO_3\right)_2}}=\dfrac{0,05}{0,2}=0,25\left(M\right)\end{matrix}\right.\)