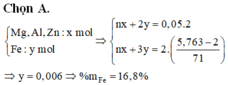Cho hỗn hợp X gồm Cu, Fe, Mg. Nếu cho 24,8g X tác dụng với Cl2 dư thì sau phản ứng thu được 75,4g hh muối khan. Mặt khác 0,3mol X tác dụng với dung dịch HCl dư thu được 5,6l h2. Tính thành phần phần trăm khối lượng Mg trong X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
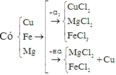
Theo định luật bảo toàn khối lượng ta có:
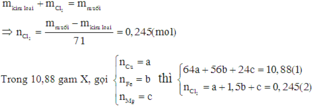
Khi cho (a + b + c) mol X tác dụng với dung dịch HCl dư thì thu được (b + c) mol H2.
Khi cho 0,44 mol X tác dụng với dung dịch HCl dư thì thu được 0,24 mol H2.
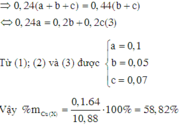

Đáp án B
Trong 10,88g X gọi số mol Cu, Fe và Mg là x, y, z
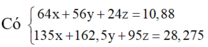
Trong 0,44 mol X có kx mol Cu, ky mol Fe và kz mol Mg (giữ đúng tỉ lệ)
Do đó kx + ky + kz = 0,44 (1)
Khi cho X tác dụng với HC1 thì
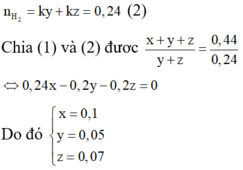
Vậy phần trăm khối lượng của Cu trong X là 58,82%

Đáp án B
Xét thì nghiệm 2:BT e có
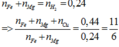 (1)
(1)
Xét thí nghiệm 1 ta có
Gọi số mol của Fe,Mg,Cu là a,b,c (mol)
Ta có 56a+24b+64c=10,08 (2)
Khối lượng muối là 28,275=>162,5a+95b+135c=28,275(vì Fe tác dụng với Cl2 tạo FeCl3) (3)
Từ 1,2,3 ta có n F e = 0,05, n C u = 0,1; n M g = 0,07
=> m C u =0,1.64=6,4(g)

Đáp án B
Xét thì nghiệm 2:BT e có
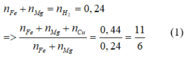
Xét thí nghiệm 1 ta có
Gọi số mol của Fe,Mg,Cu là a,b,c (mol)
Ta có 56a+24b+64c=10,08 (2)
Khối lượng muối là 28,275=>162,5a+95b+135c=28,275(vì Fe tác dụng với Cl2 tạo FeCl3) (3)
Từ 1,2,3 ta có ![]()
![]()

TN1: Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Cu}=c\left(mol\right)\end{matrix}\right.\)
=> 65a + 56b + 64c = 37 (1)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a---------------------->a
Fe + 2HCl --> FeCl2 + H2
b---------------------->b
=> \(a+b=\dfrac{8,96}{22,4}=0,4\) (2)
TN2: Gọi \(\left\{{}\begin{matrix}n_{Zn}=ak\left(mol\right)\\n_{Fe}=bk\left(mol\right)\\n_{Cu}=ck\left(mol\right)\end{matrix}\right.\)
=> ak + bk + ck = 0,15 (3)
\(n_{Cl_2}=\dfrac{3,92}{22,4}=0,175\)
PTHH: Zn + Cl2 --to--> ZnCl2
ak-->ak
2Fe + 3Cl2 --to--> 2FeCl3
bk--->1,5bk
Cu + Cl2 --to--> CuCl2
ck-->ck
=> ak + 1,5bk + ck = 0,175 (4)
(1)(2)(3)(4) => \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,2\left(mol\right)\\c=0,2\left(mol\right)\\k=0,25\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,2.65}{37}.100\%=35,135\%\\\%m_{Fe}=\dfrac{0,2.56}{37}.100\%=30,27\%\\\%m_{Cu}=\dfrac{0,2.64}{37}.100\%=34,595\%\end{matrix}\right.\)