Khử 3,04(g) hỗn hợp FeO, Fe2O3, Fe3O4, Fe cần vừa đủ 0,05 mol H2 mặt khác hòa tan 3,04g hỗn hợp trên trong dung dịch H2SO4 đặc nóng thu được V lít SO2 ở điều kiện chuẩn. Tính V
Mong mọi người giải chi tiết. Cảm ơn!!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Quy đổi hỗn hợp X về hỗn hợp hai chất FeO và Fe2O3 với số mol là x, y
Ta có:
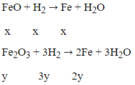
Có: x + 3y = 0,05 và 72x +160y = 3,04
⇒ x = 0,02mol; y = 0,01mol

Vậy VSO2 = 0,01 . 22,4 = 0,224 lít hay 224ml

Tách 3,04 gam hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 thành x mol Fe và y mol O
Ta có mX = 3,04 = 56x + 16y (*)
Để khử hoàn toàn 3,04 gam hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 thì cần 0,05 mol H2 tọa thành Fe và H2O => số mol O trong X sẽ = số mol O trong H2O (bảo toàn ng tố O) = 0,05 mol
=>y=0,05
Kết hợp với (*) ta đc x=0,04 mol
Áp dụng bảo toàn e (trong suốt quá tring PỨ)
Fe (0,04 mol) ----> Fe(3+) 0,04 mol => cho 0,12 mol e
O (0,05 mol) ----> O(2-) 0,05 mol => nhận 0,1 mol e
S(6+) (z mol) -----> S(4+) z mol => nhận 2z mol
=> 0,12=0,1+2z => z=0,01 mol
=> V=224 ml

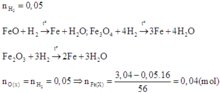
Coi hỗn hợp X ban đầu gồm Fe và O.
Khi đó áp dụng định luật bảo toàn mol electron, ta có:
![]()
Đáp án A.

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng. Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
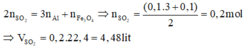

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng.Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
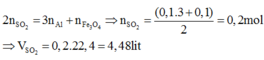

Đáp án B
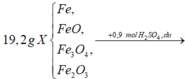
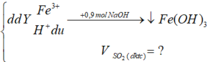
nH+ du = nNaOH - 3nFe(OH)3
=0,9 - 3.0,2 =0,3 mol
=> nH2SO4 dư = 0,3/2 = 0,15 (mol)
Coi hỗn hợp X ban đầu gồm Fe: x mol và O: y mol
Gọi nSO2 = z mol


Quy đổi thành Fe (a mol), O (b mol)
\(H_2+\left[O\right]->H_2O\\ n_O=n_{H_2}=0,05mol\\ m_{O\left(hh\right)}=16.0,05=0,8g\\ n_{Fe\left(hh\right)}=\dfrac{3,04-0,8}{56}=0,04mol\\ BT.electron:2n_{SO_2}+2n_O=3n_{Fe}\\ n_{SO_2}=\dfrac{3.0,04-2.0,05}{2}=0,01mol\\ V=22,4.0,01=2,24L\)