Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có nO(mất đi) = nCO = 0,05 (mol)
=> mhh rắn sau pư = 3,04 - 0,05.16 = 2,24(g)

Đáp án A
Quy hỗn hợp X chứa hai chất: FeO xmol và Fe2O3 y mol
Cho X+ khí CO→Chất rắn Y + khí Z chứa CO, CO2
CO2+ Ca(OH)2 → CaCO3+ H2O
Có: nCO2= nCaCO3= 0,04 mol
Cho Y + H2SO4 đặc nóng dư thu được nSO2=0,045 mol
- Quá trình cho e:
FeO → Fe3++ 1e
x x mol
C+2 → C+4+ 2e
0,04 0,08 mol
- Quá trình nhận electron:
S+6+ 2e → SO2
0,09← 0,045 mol
Theo định luật bảo toàn electron:
ne cho= ne nhận → x+0,08 = 0,09→ x= 0,01mol
Muối thu được sau phản ứng là Fe2(SO4)3
→ nFe2(SO4)3= 18/400= 0,045 mol
Bảo toàn nguyên tố Fe ta có:
x+ 2y= 0,045.2→ y= 0,04 mol
→ m= mFeO + mFe2O3=72x + 160y= 72.0,01+ 160.0,04= 7,12 gam

- Viết đúng ptpư:
\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_3\rightarrow2Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(nNO=0,04\left(mol\right)\)
Gọi nFe là x(mol) ; nCu là y(mol)
ta có hệ pt:
\(\left\{{}\begin{matrix}m_{hh}=56x+64y=3,04\\nNO=x+\dfrac{2}{3y}=0,04\end{matrix}\right.\)
Giải hệ ta được: x = 0,02 mol ; y = 0,03 mol
\(\Rightarrow mFe=0,02.56=1,12\left(g\right)\)
\(mCu=0,03.64=1,92\left(g\right)\)

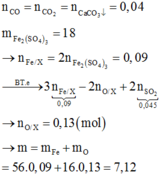

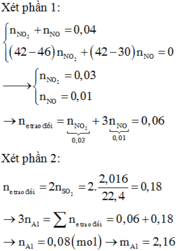
Tách 3,04 gam hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 thành x mol Fe và y mol O
Ta có mX = 3,04 = 56x + 16y (*)
Để khử hoàn toàn 3,04 gam hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 thì cần 0,05 mol H2 tọa thành Fe và H2O => số mol O trong X sẽ = số mol O trong H2O (bảo toàn ng tố O) = 0,05 mol
=>y=0,05
Kết hợp với (*) ta đc x=0,04 mol
Áp dụng bảo toàn e (trong suốt quá tring PỨ)
Fe (0,04 mol) ----> Fe(3+) 0,04 mol => cho 0,12 mol e
O (0,05 mol) ----> O(2-) 0,05 mol => nhận 0,1 mol e
S(6+) (z mol) -----> S(4+) z mol => nhận 2z mol
=> 0,12=0,1+2z => z=0,01 mol
=> V=224 ml