Đốt cháy hoàn toàn 26g bột đồng có lẫn tạp chất không cháy cần dùng 6,4g khí O2 thu được 32gam sản phẩm ( biết Cu trong sản phẩm hóa trị 2). Tính thành phần phần trăm về khối lượng của tạp chất trong lượng bột đồng trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Đặt:n_{Fe}=a\left(mol\right);n_S=b\left(mol\right)\left(a,b>0\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ \Rightarrow\left\{{}\begin{matrix}56a+32b=20\\\dfrac{44,8}{3}a+22,4b=6,72\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,1\end{matrix}\right.\\ a,\%m_{Fe}=\dfrac{0,3.56}{20}.100\%=84\%\\ \%m_S=100\%-84\%=16\%\\ b,m_{sp}=m_{hhFe,S}+m_{O_2}=20+0,3.32=29,6\left(g\right)\)
a) \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\) (mol)
Gọi x,y lần lượt là số mol của Fe và S.(x,y>0)
Theo bài ra, ta có: 56x+32y=20 (I)
PTHH: \(3Fe\) + \(2O_2\)\(\underrightarrow{t^o}\)\(Fe_3O_4\).
Theo pt: x\(\rightarrow\) \(\dfrac{2}{3}x\) \(\dfrac{1}{3}x\) (mol) (1)
PTHH: \(S+O_2\) \(\underrightarrow{t^o}\) \(SO_2\).
Theo pt: y \(\rightarrow\) y y (mol) (2)
Từ (1) và (2) \(\Rightarrow\) \(\sum n_{O_2}=\dfrac{2}{3}x+y=0,3\) (mol) (II)
Giải hệ phương trình (I) và (II) ta được \(\left\{{}\begin{matrix}x=0,3\\y=0,1\end{matrix}\right.\)
\(\Rightarrow\) \(m_{Fe}=0,3.56=16,8\left(g\right)\)
\(\Rightarrow\%m_{Fe}=\dfrac{16,8}{20}.100\%=84\%\)
\(\Rightarrow\%m_S=100\%-84\%=16\%\)
b) \(m_{Fe_3O_4}=0,1.\left(3.56+4.16\right)=23,2\left(g\right)\)
\(m_{SO_2}=0,1.\left(32+2.16\right)=6,4\left(g\right)\)

1) nh2=0,2; n CACO3=0,7
pt1: CH4+2O2 ---> CO2+2H2O
x x
pt2: C2H4 +3O2 ----> 2CO2+2H2O
y 2y
pt3: CO2+CA(OH)2 ----> CACO3+H2O
0,7 0,7
ta có hệ pt: x+y=0,2
x+2y=0,7
tự tìm
b) nbr2=1
pt: C4H6+ 2Br2 -----> C4H6Br4
0,05 0,1 0,05
tỉ lệ: 0,3/1 > 0,1/2 => C4H6 dư
CM C4H6Br2=0,05/8,72
CM C4H6 dư= 0,25/8,72

\(a,m_{C}=9,8.80\%=7,68(tấn)\\ m_{\text{tạp chất}}=9,6-7,68=1,92(tấn)\\ b,PTHH:C+O_2\xrightarrow{t^o}CO_2\\ c,n_{C}=\dfrac{7680}{12}=640(kmol)\\ \Rightarrow n_{CO_2}=640(kmol)\\ \Rightarrow m_{CO_2}=640.44=28160(kg)=28,16(tấn)\)

a)
Gọi số mol C2H5OH, CH3COOH là a, b (mol)
\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\); \(n_{CaCO_3}=\dfrac{40}{100}=0,4\left(mol\right)\)
PTHH: C2H5OH + 3O2 --to--> 2CO2 + 3H2O
a----->3a-------->2a
CH3COOH + 2O2 --to--> 2CO2 + 2H2O
b------>2b-------->2b
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,4<----0,4
=> \(\left\{{}\begin{matrix}3a+2b=0,5\\2a+2b=0,4\end{matrix}\right.\) => a = 0,1 (mol); b = 0,1 (mol)
a = 0,1.46 + 0,1.60 = 10,6 (g)
b) \(\left\{{}\begin{matrix}\%m_{C_2H_5OH}=\dfrac{0,1.46}{10,6}.100\%=43,4\%\\\%m_{CH_3COOH}=\dfrac{0,1.60}{10,6}.100\%=56,6\%\end{matrix}\right.\)
c)
PTHH: 2CH3COOH + Na2CO3 --> 2CH3COONa + CO2 + H2O
0,1----------------------------------->0,05
B là khí CO2
V = 0,05.22,4 = 1,12 (l)

PTHH: \(C+O_2\xrightarrow[]{t^o}CO_2\)
Tính theo sản phẩm
Ta có: \(n_C=n_{CO_2}=\dfrac{264}{44}=6\left(mol\right)\)
\(\Rightarrow\%m_C=\dfrac{12\cdot6}{120}\cdot100\%=60\%\) \(\Rightarrow\%_{tạp.chất}=40\%\)
\(n_{CO_2}=\frac{264}{44}=6(mol)\\ C+O_2\buildrel{{t^o}}\over\longrightarrow CO_2\\ n_{C}=n_{CO_2}=6(mol)\\ m_{C}=6.12=72(g)\\ \%m_{\text{tạp chât}}=\frac{120-72}{120}.100\%=40\%\)

Khi A tác dụng với O 2 chỉ sinh ra, và H 2 O , vậy A có chứa cacbon, hiđro, có thể có hoặc không có oxi.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m A + m O 2 = 7,30 (g) (1)
Theo đầu bài: m C O 2 + m H 2 O = 3,70(g). (2)
Từ hệ (1) và (2), tìm được m C O 2 = 5,50 g; m H 2 O = 1,80 g.
Khối lượng C trong 5,50 g
C
O
2
: 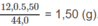
Khối lượng H trong 1,8 g
H
2
: 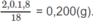
Đó cũng là khối lượng c và H trong 2,50 g chất A. Vậy chất A phải chứa O.
Khối lượng O trong 2,50 g A: 2,50 - 1,50 - 0,200 = 0,80 (g)
Phần trăm khối lượng của C: 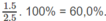
Phần trăm khối lương của H: 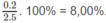
Phần trăm khối lương của O: 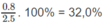
Theo ĐLBT KL, có: mCu + mO2 = mCuO
⇒ mCu = mCuO - mO2 = 32 - 6,4 = 25,6 (g)
⇒ m tạp chất = 26 - 25,6 = 0,4 (g)
\(\Rightarrow\%m_{tapchat}=\dfrac{0,4}{26}.100\%\approx1,54\%\)