Hoà tan 12,8 g hh Fe và FeO bằng dd h2so4 loãng vua du thu đ 2,24 lít đktc thành phần phần trăm theo khỏi lượng FeO trong hh là
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

UT
24 tháng 8 2021
a, gọi a= nFe
b= nFeO
=> 56a + 72b= 12,8 (1)
Fe +H2SO4 -> FeSO4 +H2
a b b a
FeO +H2SO4 -> FeSO4 +H2O
b b b
a=nH2 = 2,24/22,4= 0,1 mol
từ (1) => b= 0,1
mFe= 56.0,1=5,6(g)
m FeO = 72.0,1= 7,2(g)
b, nH2SO4 (bđ) = 0,25 mol
nH2SO4 pứ = a+b =0,2 mol
=> nH2SO4 dư = 0,25-0,2=0,05 mol
2NaOH +H2SO4 -> Na2SO4 +2H2O
0,1 0,05
V(NaOH)= 0,1/ 1= 0,1 lit =100ml
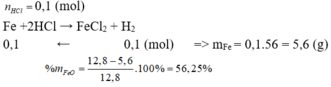
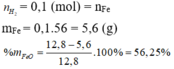



\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
0,1 0,1
\(m_{Fe}=0,1.56=5,6\left(g\right)\\ \%m_{Fe}=\dfrac{5,6}{12,8}=43,75\%\\ \%m_{FeO}=100\%-43,75\%=56,25\%\)