Đốt cháy hết m gam than chứa 4% tạp chất trơ trong V lít khí O2 (đktc) thu được hỗn hợp A gồm 2 khí có tỷ khối so với H2 bằng 19,6. Cho toàn bộ hỗn hợp A lội từ từ qua 300 ml dung dịch chứa Ba(OH)2 0,1 M thu được 3,94 gam kết tủa. Tính giá trị của m và V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


đề đáng lẽ phải là tính a với V1 chứ :v
\(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,3.0,1=0,03\left(mol\right)\\n_{KOH}=0,3.0,2=0,06\left(mol\right)\end{matrix}\right.\)
\(n_{BaCO_3}=\dfrac{3,94}{197}=0,02\left(mol\right)\)
- TH1: Kết tủa không bị hòa tan
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,02<----0,02
=> nCO2 = 0,02 (mol)
- Nếu trong hỗn hợp A chứa CO2, O2 dư
\(\overline{M}_A=\dfrac{0,02.44+32.n_{O_2}}{0,02+n_{O_2}}=19,6.2=39,2\left(g/mol\right)\)
=> nO2(dư) = \(\dfrac{1}{75}\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,02<-0,02<---0,02
=> \(V_1=\left(\dfrac{1}{75}+0,02\right).22,4=\dfrac{56}{75}\left(l\right)\)
\(m_C=0,02.12=0,24\left(g\right)\)
=> \(a=m_{than}=\dfrac{0,24.100}{96}=0,25\left(g\right)\)
- Nếu trong hỗn hợp chứa CO2, CO
\(\overline{M}=\dfrac{0,02.44+28.n_{CO}}{0,02+n_{CO}}=39,2\left(g/mol\right)\)
=> \(n_{CO}=\dfrac{3}{350}\left(mol\right)\)
Bảo toàn C: \(n_C=0,02+\dfrac{3}{350}=\dfrac{1}{35}\left(mol\right)\)
=> \(m_C=\dfrac{1}{35}.12=\dfrac{12}{35}\left(g\right)\)
Bảo toàn O: \(n_{O_2}=\dfrac{0,02.2+\dfrac{3}{350}}{2}=\dfrac{17}{700}\left(mol\right)\)
=> \(V_1=\dfrac{17}{700}.22,4=0,544\left(l\right)\)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,03----->0,03---->0,03
2KOH + CO2 --> K2CO3 + H2O
0,06-->0,03---->0,03
K2CO3 + CO2 + H2O --> 2KHCO3
0,03--->0,03
BaCO3 + CO2 + H2O --> Ba(HCO3)2
0,01--->0,01
=> nCO2 = 0,1 (mol)
- Nếu trong A chứa CO2, O2 dư
\(\overline{M}_A=\dfrac{0,1.44+32.n_{O_2}}{0,1+n_{O_2}}=39,2\left(g/mol\right)\)
=> \(n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,1<-0,1<------0,1
=> \(m_C=0,1.12=1,2\left(g\right)\)
=> \(a=m_{than}=\dfrac{1,2.100}{96}=1,25\left(g\right)\)
\(V_1=\left(\dfrac{1}{15}+0,1\right).22,4=\dfrac{56}{15}\left(l\right)\)
- Nếu trong A chứa CO2, CO
\(\overline{M}_A=\dfrac{0,1.44+28.n_{CO}}{0,1+n_{CO}}=39,2\left(g/mol\right)\)
=> \(n_{CO}=\dfrac{3}{70}\left(mol\right)\)
Bảo toàn C: \(n_C=0,1+\dfrac{3}{70}=\dfrac{1}{7}\left(mol\right)\)
=> \(m_C=\dfrac{1}{7}.12=\dfrac{12}{7}\left(g\right)\)
=> \(a=m_{than}=\dfrac{\dfrac{12}{7}.100}{96}=\dfrac{25}{14}\left(g\right)\)
Bảo toàn O: \(n_{O_2}=\dfrac{2.0,1+\dfrac{3}{70}}{2}=\dfrac{17}{140}\left(mol\right)\)
=> \(V_1=\dfrac{17}{140}.22,4=2,72\left(l\right)\)

$n_{Ba(OH)_2}= 0,2(mol)$
$n_{BaCO_3} = 0,15(mol)$
TH1 : $Ba(OH)_2$ dư
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
$n_{CO_2} = n_{BaCO_3} = 0,15(mol) > n_{hh\ khí} = 0,05$(loại)
TH2 : Kết tủa bị hòa tan 1 phần
$n_{Ba(HCO_3)_2} = n_{Ba(OH)_2} - n_{BaCO_3} = 0,05(mol)$
$n_{CO_2} = n_{BaCO_3} + 2n_{Ba(HCO_3)_2} = 0,3(mol) >n_{hh}$
(Sai đề)

Đáp án B
Đặt nN2 = x; nH2 = y ⇒ nA = x + y = 0,05 mol; mA = 28x + 2y = 0,05 × 11,4 × 2
Giải hệ có: x = 0,04 mol; y = 0,01 mol || nO/khí = 2.∑n(NO2, O2) . Bảo toàn nguyên tố Oxi:
nO/H2O = 0,25 × 6 - 0,45 × 2 = 0,6 mol. Bảo toàn nguyên tố Hidro: nNH4+ = 0,02 mol.
nCl–/Z = nHCl = 1,3 mol. Bảo toàn điện tích: nMg2+ = (1,3 - 0,25 × 2 - 0,02)/2 = 0,39 mol.
⇒ m = 0,39 × 24 + 0,25 × 64 + 0,02 × 18 + 1,3 × 35,5 = 71,87(g)

Đáp án C
MY = 16,7 => chứng tỏ H2 dư
Y gồm C3H8 và H2; nY = 0,01 mol => nC3H8 = 0,0035; nH2 = 0,0065 mol
nCa(OH)2 = 0,006 mol => nOH = 0,012 mol
Đốt cháy X thì tạo sản phẩm với lượng giống như đốt cháy Y
=> nCO2 = 3nC3H8 = 0,0105 mol; nH2O = 0,0205 mol
=> nCaCO3 = nOH – nCO2 = 0,0015 mol
=> mCaCO3 – (mCO2 + mH2O) = - 0,681g
=> m dung dịch tăng 0,681g

Đáp án C
MY = 16,7 => chứng tỏ H2 dư
Y gồm C3H8 và H2 ; nY = 0,01 mol
=> nC3H8 = 0,0035 ; nH2 = 0,0065 mol
nCa(OH)2 = 0,006 mol => nOH = 0,012 mol
Đốt cháy X thì tạo sản phẩm với lượng giống như đốt cháy Y
=> nCO2 = 3nC3H8 = 0,0105 mol ; nH2O = 0,0205 mol
=> nCaCO3 = nOH – nCO2 = 0,0015 mol
=> mCaCO3 – (mCO2 + mH2O) = - 0,681g
=> m dung dịch tăng 0,681g

Đáp án C
MY = 16,7 => chứng tỏ H2 dư
Y gồm C3H8 và H2 ; nY = 0,01 mol
=> nC3H8 = 0,0035 ; nH2 = 0,0065 mol
nCa(OH)2 = 0,006 mol => nOH = 0,012 mol
Đốt cháy X thì tạo sản phẩm với lượng giống như đốt cháy Y
=> nCO2 = 3nC3H8 = 0,0105 mol ; nH2O = 0,0205 mol
=> nCaCO3 = nOH – nCO2 = 0,0015 mol
=> mCaCO3 – (mCO2 + mH2O) = - 0,681g
=> m dung dịch tăng 0,681g

Đáp án : C
MY = 16,7 => chứng tỏ H2 dư
Y gồm C3H8 và H2 ; nY = 0,01 mol
⇒ n C 3 H 8 = 0 , 0035 ; n H 2 = 0 , 0065 m o l
⇒ n C a O H 2 = 0 , 006 m o l , n H 2 = 0 , 012 m o l
Đốt cháy X thì tạo sản phẩm với lượng giống như đốt cháy Y
⇒ n C O 2 = 3 n C 3 H 8 = 0 , 0105 m o l
n H 2 O = 0 , 0205 m o l
⇒ n C a C O 3 = n O H - n C O 2 = 0 , 0015 m o l
⇒ m C a C O 3 - m C O 2 + m H 2 O = - 0 , 681 g
=> m dung dịch tăng 0,681g

Ta có sơ đồ phản ứng:
m(gam) (Mg, Fe) + --O2→ (m+4,16) gam B + --HCl→ D (Mg2+ x mol; Fe2+ y mol; Fe3+ z mol); Cl-)
D + --AgNO3→ (11m – 12,58) gam (Ag + AgCl)
Ta có m(O) = 4,16 gam → n(O) = 0,26 mol → n(Cl- trong D) = 0,52 mol
→ n(AgCl) = 0,52 mol
Ta có hệ phương trình
(1): 24x + 56(y+z) = m
(2) ĐLBT điện tích: 2x+2y+ 3z = 0,52
(3) m + 0,52*35,5 = 4m-6,5
→ m = 8,32 gam → n(Ag) = 0,04 = y → x = 0,16; z = 0,04
Mặt khác trong 4,5m gam A có: Mg = 0,72 mol và Fe 0,36 mol
Dung dịch muối: Mg2+: 0,72 mol; Fe3+: 0,36mol; NH4+: t mol; NO3-: q mol
hợp khí F gồm N2 (0,04 mol) và N2O (0,04 mol)
Áp dụng ĐLBT mol e: → t = 0,225 mol
Áp dụng ĐLBT điện tích → q = 2,745 mol → m 211,68 gam → Đáp án C

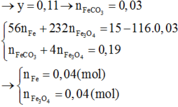
\(n_{Ba\left(ỌH\right)_2}=0,1.0,3=0,03\left(mol\right)\\ n_{BaCO_3}=\dfrac{3,94}{197}=0,02\left(mol\right)\)
PTHH:
Ba(OH)2 + CO2 ---> BaCO3 + H2O
0,02 0,02 0,02
So sánh: 0,2 < 0,3 => Có tạo muối axit
\(n_{Ba\left(OH\right)_2\left(tạo.muối.axit\right)}\) = 0,03 - 0,02 = 0,01 (mol)
Ba(OH)2 + CO2 + H2O ---> Ba(HCO3)2
0,01 0,01
=> nCO2 = 0,02 + 0,01 = 0,03 (mol)
PTHH: C + O2 ---to---> CO2
0,03 0,03 0,03
mC = 0,03.12 = 0,36 (g)
=> m = mthan = \(\dfrac{0,36}{100\%-4\%}=0,375\left(g\right)\)
Gọi nO2 (dư) = a (mol)
=> \(M_A=\dfrac{0,03.44+32a}{0,03+a}=19,6.2\\ \Leftrightarrow a=0,02\left(mol\right)\)
=> VO2 = (0,03 + 0,02).22,4 = 1,12 (l)
phương trình 2 quên cân bằng ạ