Để đốt cháy hoàn toàn hỗn hợp X gồm 0,1 mol Al và 0,05 mol Mg cần dùng một lượng hỗn hợp khí Y gồm 0,05 mol O2 và x mol khí Cl2. Sau khi phản ứng xong, thu được m gam chất Z. Giá trị của m là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


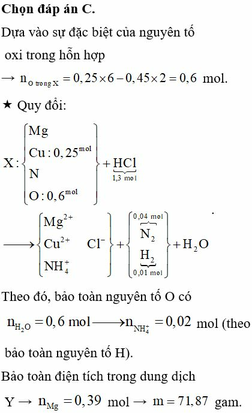
Đáp án C
Đặt ![]()
![]()
![]()
Bảo toàn nguyên tố Oxi:
![]()
Bảo toàn nguyên tố Hidro:
![]()
Bảo toàn điện tích:
![]()
![]()

Giải thích:
Vì Mx = 12,2.2 = 24,4 hỗn hợp khí là NO và H2

Al + 4H+ + NO3- → Al3+ + NO + H2O
0,1 ← 0,4 ← 0,1 ← 0,1
2Al + 6H+ → 2Al3+ + 3H2
1/60 ← 0,05 ← 0,025
Bảo toàn khối lượng m = m Al + m Na+ + m K+ + m NO3- + m Cl-
= ( 0,1 + 1/60) .27 + 23. 0,05 + 0,1.39 + (0,15 – 0,1). 62 + 0,45.35,5
= 27,275 (g)
Đáp án B

Đáp án B
MY = 24,4 ⇒ Y chứa H2 và NO. Đặt nH2 = x mol; nNO = y mol
⇒ nY = x + y = 0,125 mol
mY = 2x + 30y = 0,125 × 24,4.
Giải hệ có: x = 0,025 mol; y = 0,1 mol.
Do Y chứa H2 ⇒ X không chứa NO3–.
Bảo toàn nguyên tố Nitơ:
nNH4+ = 0,05 + 0,1 – 0,1 = 0,05 mol.
Bảo toàn electron: 3nAl phản ứng = 2nH2 + 3nNO + 8nNH4+
⇒ nAl phản ứng = 0,25 mol. X chứa AlCl3, NaCl, KCl, NH4Cl
⇒ m = 0,25 × 133,5 + 0,05 × 58,5 + 0,1 × 74,5 + 0,05 × 53,5 = 46,425 gam

Chọn đáp án B
MY = 24,4 ⇒ Y chứa H2 và NO. Đặt nH2 = x mol; nNO = y mol ⇒ nY = x + y = 0,125 mol
mY = 2x + 30y = 0,125 × 24,4. Giải hệ có: x = 0,025 mol; y = 0,1 mol.
Do Y chứa H2 ⇒ X không chứa NO3–. Bảo toàn nguyên tố Nitơ:
nNH4+ = 0,05 + 0,1 – 0,1 = 0,05 mol. Bảo toàn electron: 3nAl phản ứng = 2nH2 + 3nNO + 8nNH4+
⇒ nAl phản ứng = 0,25 mol. X chứa AlCl3, NaCl, KCl, NH4Cl
⇒ m = 0,25 × 133,5 + 0,05 × 58,5 + 0,1 × 74,5 + 0,05 × 53,5 = 46,425 gam.
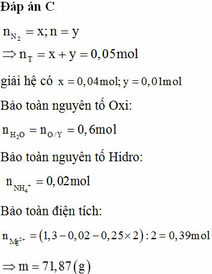
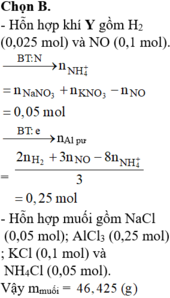



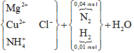

BT e: \(3n_{Al}+2n_{Mg}=4n_{O_2}+2n_{Cl_2}\)
\(\Rightarrow3\cdot0,1+2\cdot0,05=4\cdot0,05+2\cdot x\)
\(\Rightarrow x=0,1mol\)
\(m=m_{Al}+m_{Mg}+m_{O_2}+m_{Cl_2}\)
\(=0,1\cdot27+0,05\cdot24+0,05\cdot2\cdot16+0,1\cdot35,5\cdot2\)
\(=12,6g\)
Theo bảo toàn electron ta có: \(3\cdot n_{Al}+2\cdot n_{Mg}=2\cdot n_{Cl_2}+4\cdot N_{O_2}\)
\(\Rightarrow3\cdot0,1+2\cdot0,05=4\cdot0,05+2x\Rightarrow x=0,2\)
\(\Rightarrow m_Z=m_X+m_Y=0,1\cdot27+0,05\cdot24+0,05\cdot32+0,2\cdot71=19,7g\)