Cho 4,6 g Na tác dụng với 4,48 lít khí Cl2 ở điều kiện tiêu chuẩn thu được m gam muối NaCl
a, Chất nào dư và dư bao nhiêu gam
b, Tính khối lượng muối thu được bnhiu
(biết a = 23 CL = 3,35)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\\ n_{Cl_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ Mg+Cl_2\rightarrow\left(t^o\right)MgCl_2\\ a,Vì:\dfrac{0,2}{1}< \dfrac{0,3}{1}\Rightarrow Mgdư\\n_{Mg\left(p.ứ\right)}=n_{MgCl_2}=n_{Cl_2}=0,2\left(mol\right)\\ \Rightarrow n_{Mg\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\\ m_{Mg\left(dư\right)}=0,1.24=2,4\left(g\right)\\ b,m_{MgCl_2}=0,2.95=19\left(g\right)\)
\(n_{Mg}=\dfrac{m}{M}=\dfrac{7,2}{24}=0,3\) (mol)
\(n_{Cl_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\)(mol)
PTHH : Mg + Cl2 ---> MgCl2
1 : 1 : 1
Dễ thấy : \(\dfrac{n_{Mg}}{1}>\dfrac{n_{Cl_2}}{1}\)
=> Mg dư 0,1 mol
=> \(m_{Mg}=n.M=0,1.24=2,4\left(g\right)\)
=> \(n_{MgCl_2}=0,2\left(mol\right)\) => \(m_{MgCl_2}=n.M=0,2.\left(24+71\right)=19\left(g\right)\)
\(n_{Mg}=\dfrac{m}{M}=\dfrac{7,2}{24}=0,3\) (mol)
\(n_{Cl_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\)(mol)
PTHH : Mg + Cl2 ---> MgCl2
1 : 1 : 1
Dễ thấy : \(\dfrac{n_{Mg}}{1}>\dfrac{n_{Cl_2}}{1}\)
=> Mg dư 0,1 mol
=> \(m_{Mg}=n.M=0,1.24=2,4\left(g\right)\)
=> \(n_{MgCl_2}=0,2\left(mol\right)\) => \(m_{MgCl_2}=n.M=0,2.\left(24+71\right)=19\left(g\right)\)

\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PT: \(2Na+H_2SO_4\rightarrow Na_2SO_4+H_2\)
Theo PT: \(n_{Na_2SO_4}=n_{H_2}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)

Fe (0,2 mol) + S \(\underrightarrow{t^o}\) FeS (0,2 mol).
Khối lượng muối FeS thu được là 0,2.88=17,6 (g).
FeS (0,2 mol) + 2HCl → FeCl2 + H2S\(\uparrow\) (0,2 mol).
Thể tích khí thu được ở đktc là 0,2.22,4=4,48 (lít).

a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
b) Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\\n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,5}{1}>\dfrac{0,1}{2}\) \(\Rightarrow\) HCl phản ứng hết, Zn còn dư
\(\Rightarrow n_{Zn\left(dư\right)}=0,5-0,05=0,45\left(mol\right)\) \(\Rightarrow m_{Zn\left(dư\right)}=0,45\cdot65=29,25\left(g\right)\)
c+d) Theo PTHH: \(n_{ZnCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,05mol\)
\(\Rightarrow\left\{{}\begin{matrix}m_{ZnCl_2}=0,05\cdot136=6,8\left(g\right)\\V_{H_2}=0,05\cdot22,4=1,12\left(l\right)\end{matrix}\right.\)

Chọn đáp án C
Giả sử ancol có n chức

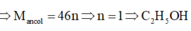
Giả sử axit có m chức
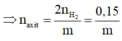
![]()
![]()

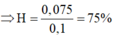
\(a,n_{Na}=\dfrac{m_{Na}}{M_{Na}}=\dfrac{4,6}{23}=0,2\left(mol\right)\\ n_{Cl_2}=\dfrac{V_{Cl_2\left(đktc\right)}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ PTHH:2Na+Cl_2\rightarrow2NaCl\\ Vì:\dfrac{0,2}{2}< \dfrac{0,2}{1}\Rightarrow Cl_2dư\\ \Rightarrow n_{Cl_2\left(dư\right)}=0,2-\dfrac{0,2}{2}=0,1\left(mol\right)\\ \Rightarrow m_{Cl_2\left(dư\right)}=0,1.71=7,1\left(g\right)\\ b,n_{NaCl}=n_{Na}=0,2\left(mol\right)\\ \Rightarrow m_{NaCl}=58,5.0,2=11,7\left(g\right)\)