Cho 12,9 gam hỗn hợp X gồm Al và Al2O3 vào 400 ml dung dịch NaOH 1M, đun nóng. Sau phản ứng hoàn toàn thu được dung dịch Y và thấy thoát ra 3,36 lít H2 (đktc). Thêm 150 ml dung dịch H2SO4 1M vào dung dịch Y, thu được kết tủa có khối lượng là
A. 15,6 gam.
B. 23,4 gam.
C. 19,5 gam.
D. 7,8 gam.


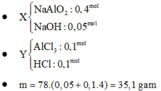

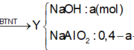
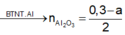
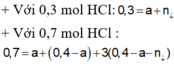
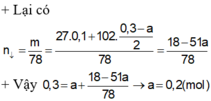


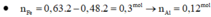
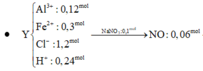
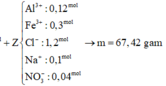
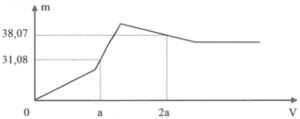
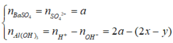
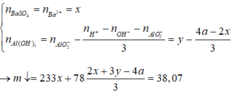
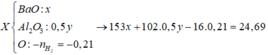
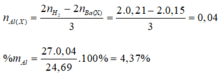
Đáp án A