Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Ta có: nNaOH = 0,15 mol; nBa(OH)2 = 0,05 mol
Dung dịch Y chứa 0,15 mol Na+, 0,05 mol Ba2+, u mol AlO2- và v mol OH- dư
Định luật bảo toàn điện tích ta có u + v = 0,15 + 0,05.2 = 0,25 (1)
Ta có: nHCl = 0,32 mol và nH2SO4 = 0,04 mol→ nH+ = 0,4 mol; nSO4(2-) = 0,04 mol
→ nBaSO4 = 0,04 mol
Ta có: mkết tủa = 21,02 gam → nAl(OH)3 = 0,15 mol
Nếu Al(OH)3 chưa bị hòa tan thì nH+ = 0,4 = v + 0,15 (2)
Nếu Al(OH)3 đã bị hòa tan thì nH+ = 0,4 = v + 4u - 3.0,15 (3)
Giải hệ (1) và (2) ra vô nghiệm
Giải hệ (1) và (3) ra u = 0,2 và v = 0,05
Vậy Y gồm Na+ 0,15 mol; 0,05 mol Ba2+; 0,2 mol AlO2- và OH- dư (0,05 mol)
V lít dung dịch Z gồm 0,64V mol HCl và 0,08V mol H2SO4
→ nH+ = 0,8V mol và nSO4(2-) = 0,08 V mol
Khi Al(OH)3 max thì 0,8V = u+ v suy ra V = 0,3125
Suy ra nBaSO4 = 0,025 mol → mkết tủa = 21,425 gam
Khi BaSO4 max thì 0,08V = 0,05 suy ra V = 0,625
Suy ra nH+ = 0,8V = v + 4u-3.nAl(OH)3 → nAl(OH)3 = 7/60 mol → mkết tủa = 20,75 gam
Vậy mkết tủa max = 21,425 gam

Đáp án A
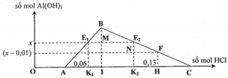
Gọi số mol của Ba2+, AlO2- và OH- lần lượt là x, y và 2x-y.
Các giai đoạn của phản ứng:
Ba(OH)2+H2SO4 → BaSO4(kt) +2H2O
Ba(AlO2)+ H2SO4+ 2H2O → BaSO4(kt)+2Al(OH)3(kt)
2Al(OH)3(kt)+3 H2SO4 → Al2(SO4)3+3 H2O
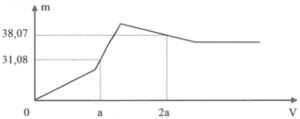
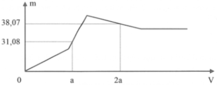
- Xét thời điểm V=a, ta có:
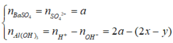
→ m k t = 233 a + 78 ( 2 a - 2 x + y ) = 31 , 08
- Xét thời điểm V=2a, ta có:
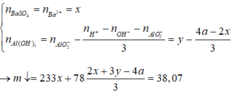
Quy đổi hỗn hợp X kết hợp với sử dụng bảo toàn e, ta có:
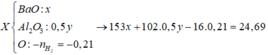
Giải hệ ba phương trình, ta có: a=0,12, x=0,15; y=0,1
Sử dụng bảo toàn e, ta có:
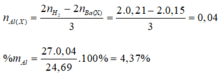

Đáp án B
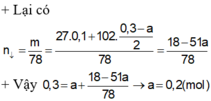
+ S ơ đ ồ p h ả n ứ n g : A l : 2 n H 2 3 = 0 , 1 m o l A l 2 O 3 : x m o l ⏟ m = ( 2 , 7 + 102 x ) g a m → N a O H : 0 , 4 m o l n N a A l O 2 = 0 , 1 + 2 x n N a O H = 0 , 3 - 2 x ⏟ d d Y + H 2 ↑ ⏟ 0 , 15 m o l N a A l O 2 N a O H ⏟ d d Y + 0 , 3 y m o l H C l ( T N 1 ) 0 , 7 y m o l H C l ( T N 2 ) → m g a m A l ( O H ) 3 ↓ ⏟ 2 , 7 + 102 x 78 m o l + . . . ⇒ T N 1 : A l ( O H ) 3 c h ư a b ị tan T N 2 : A l ( O H ) 3 đ ã b ị tan ⇒ T N 1 : n H + = n O H - + n A l ( O H ) 3 T N 2 : n H + = n O H - + n A l O 2 - + 3 ( n A l O 2 - - n A l ( O H ) 3 ) ⇒ 0 , 3 y = ( 0 , 3 - 2 x ) + 2 , 7 + 102 x 78 0 , 7 y = ( 0 , 3 - 2 x ) + ( 0 , 1 + 2 x ) + 3 ( 0 , 1 + 2 x ) - 2 , 7 + 102 x 78 ⇒ x = 0 , 05 y = 0 , 1 ⇒ m = 7 , 8 g ầ n n h ấ t v ớ i 8

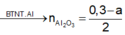
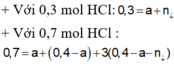
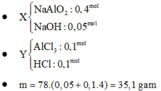







Đáp án : D
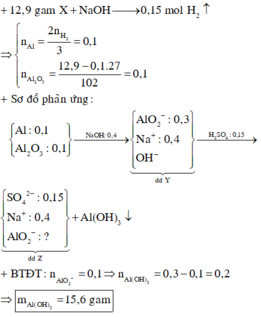
nH2= 0,15 mol ; nNaOH = 0,4 mol
Do phản ứng hoàn toàn tạo dung dịch Y => Al , Al2O3 hết
=> nAl = 2/3 nH2 = 0,1 mol => nAl2O3 = 0,1 mol
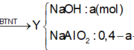
=> Dung dịch Y gồm : 0,3 mol NaAlO2 và 0,1mol NaOH
, nH2SO4 = 0,15 mol => nH+ = 0,3 mol
=> nAl(OH)3 = nH+ - nNaOH = 0,2 mol
=> mkết tủa = 15,6g