Cho 4,48lít CO đktc đi qua ống sứ nung nóng đựng 8g một oxit của Fe đến phản ứng hoàn toàn . Khí thu được sau phản ứng có tỉ khối so với H2 là 20 . Tìm oxit của Fe và % thể tích CO2 trong hỗn hợp sau phản ứng
A. Fe3O4 và 75%
B. Fe2O3 và 65%
C. FeO và 75%
D. Fe2O3 và 75%


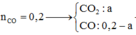
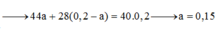
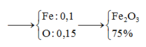



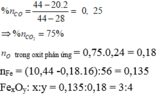

nCO =0,2
Hỗn hợp khí thu được gồm CO dư và CO2 có M = 40
Bảo toàn C ta có: n CO ban đầu = n CO dư + n CO2 = 0,2 mol
Sử dụng sơ đồ đường chéo ta có: n CO = 0,05 mol; n CO2 = 0,15 mol
⇒ %VCO2 = 75%
Ta có: CO + Ooxit → CO2
⇒ nO/Oxit = nCO2 = 0,15 mol
moxit = mFe + mO = 8g ⇒ nFe = (8 – 0,15.16)÷56 = 0,1
⇒nFe ÷ nO/oxit = 2 : 3
⇒ Oxit đó là Fe2O3
Đáp án D.