Cho V lít khí SO2 (ở đktc) vào 700 ml Ca(OH)2 0,1M sau phản ứng thu được 6 gam kết tủa. . Giá trị của V là
A. 2,24 lít hoặc 1,12 lít
B. 1,68 lít hoặc 2,016 lít
C. 2,016 lít hoặc 1,12 lít
D. 3,36 lít
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đổi: \(100ml=0,1l\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\left(1\right)\)
0,06 0,06 0,06 (mol)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\left(2\right)\)
0,08 0,04 (mol)
\(n_{Ca\left(OH\right)_2}=1.0,1=0,1\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{6}{100}=0.06\left(mol\right)\)
\(n_{Ca\left(OH\right)_2\left(2\right)}=0,1-0,06=0,04\left(mol\right)\)
\(\Rightarrow n_{CO_2}=0,06+0,04.2=0,14\left(mol\right)\)
\(\Rightarrow V_{CO_2}=n_{CO_2}.22,4=0,14.22,4=3,136\left(l\right)\)

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: \(C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\)
0,05<-----------0,1
\(\Rightarrow V=V_{C_2H_4}=0,05.22,4=1,12\left(l\right)\)
Chọn A

Câu 7: \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right);n_S=\dfrac{0,32}{32}=0,01\left(mol\right)\)
\(Al\rightarrow Al^{3+}+3e\) \(8H^++SO_4^{2-}+6e\rightarrow S+4H_2O\)
\(4H^++SO_4^{2-}+2e\rightarrow SO_2+2H_2O\)
Bảo toàn e : \(n_{SO_2}.2+n_S.6=n_{Al}.3\)
=> \(n_{SO_2}=\dfrac{0,1.3-0,01.6}{2}=0,12\left(mol\right)\)
=> \(V_{SO_2}=2,688\left(l\right)\)
\(n_{H_2SO_4}=\dfrac{0,01.8+0,12.4}{2}=0,28\left(mol\right)\)
Mình bị nhầm chỗ số mol H2SO4 nha
Sửa lại : \(n_{H^+}=4n_{SO_2}=0,6\left(mol\right)\)
Do H2SO4 ---------> 2H+ + SO42-
=> \(n_{H_2SO_4}=\dfrac{1}{2}n_{H^+}=0,3\left(mol\right)\)

1.
\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0.075\left(mol\right)\)
\(T=\dfrac{0.1}{0.075}=1.33\)
=> Tạo ra 2 muối
\(n_{CaCO_3}=a\left(mol\right),n_{Ca\left(HCO_3\right)_2}=b\left(mol\right)\)
Khi đó :
\(a+b=0.075\)
\(a+2b=0.1\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.05\\b=0.025\end{matrix}\right.\)
\(m_{sp}=0.05\cdot100+0.025\cdot162=9.05\left(g\right)\)
2.
\(n_{CO_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0.2\cdot0.2=0.04\left(mol\right)\)
\(T=\dfrac{0.005}{0.04}=1.25\)
=> Tạo ra 2 muối
\(n_{BaCO_3}=a\left(mol\right),n_{Ba\left(HCO_3\right)_2}=b\left(mol\right)\)
Ta có :
\(a+b=0.04\)
\(a+2b=0.05\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.03\\b=0.01\end{matrix}\right.\)
\(m_{BaCO_3}=0.03\cdot197=5.91\left(g\right)\)

Chọn C

S O 2 hết, Ca( O H ) 2 dư, phản ứng tạo muối CaS O 3
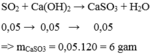

Đáp án C
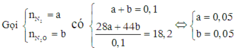
Vì khi cho dung dịch NaOH vào dung dịch B có xuất hiện khí nên sản phẩm khử có chứa NH4NO3.

Vì cho dung dịch NaOH dư vào dung dịch B nên kết tủa thu được chỉ có Mg(OH)2 (Al(OH)3 tạo thành bị tan trong kiềm dư).
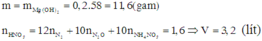
Chọn đáp án C