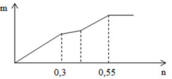
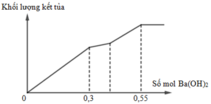
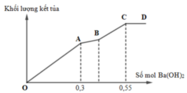
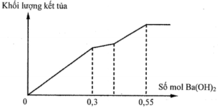
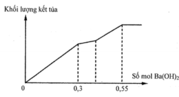
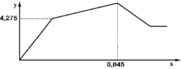
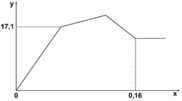
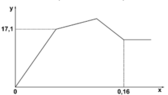
Cho từ từ từng giọt dung dịch Ba(OH)2 loãng đến dư vào dung dịch chứa a mol Al2(SO4)3 và b mol Na2SO4. Khối lượng kết tủa (m gam) thu được phụ thuộc vào số mol Ba(OH)2 (n mol) được biểu diễn theo đồ thị như hình sau
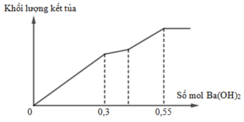
Giá trị tỉ lệ a : b tương ứng là
A. 1 : 1.
B. 2 : 3.
C. 1 : 2.
D. 2 : 5.

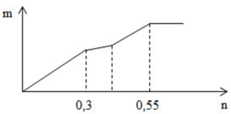
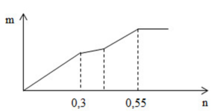

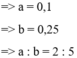
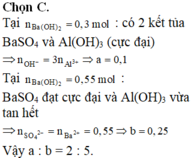
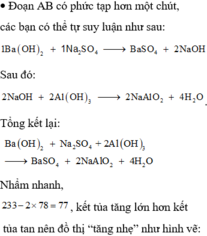



Đáp án D
· Đoạn OA biểu diễn tỉ lệ phản ứng: 3 B a ( O H ) 2 + A l 2 ( S O 4 ) 3 → 3 B a S O 4 ↓ + 2 A l ( O H ) 3
· Đoạn AB có phức tạp hơn một chút, các bạn có thể tự suy luận như sau:
B a ( O H ) 2 + N a 2 S O 4 → BaSO 4 + 2 NaOH
Sau đó: 2 N a O H + 2 A l ( O H ) 3 → 2 N a A l O 2 + 4 H 2 O
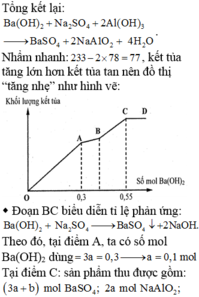
Tổng kết lại: B a ( O H ) 2 + N a 2 S O 4 + 2 A l ( O H ) 3 → B a S O 4 + N a A l O 2 + 4 H 2 O
Nhẩm nhanh, 233-2*78=77, kết tủa tăng lớn hơn kết tủa tan nên đồ thị “tăng nhẹ” như hình vẽ:
· Đoạn BC biểu diễn tỉ lệ phản ứng: B a ( O H ) 2 + N a 2 S O 4 → B a S O 4 ↓ + 2 N a O H
Theo đó, tại điểm A, ta có số mol Ba(OH)2 dùng = 3a = 0,3 ® a = 0,1 mol.
Tại điểm C, sản phẩm thu được gồm: (3a + b) mol BaSO4; 2a mol NaAlO2; (2b – 2a) mol NaOH.
Theo đó, bảo toàn nguyên tố Ba có số mol Ba(OH)2 dùng = 3a + b = 0,55 ® b = 0,25 mol.
Vậy, tỉ lệ a : b = 0,1 ¸ 0,25 = 2 ¸ 5