1. Cho 19,2 gam kim loại M tan hoàn toàn trong dung dịch HNO3 dư, thu được 4,48 lít khí NO (đktc). Cho NaOH dư vào dung dịch ta thu được một kết tủa. Nung kết tủa trong không khí đến khối lượng không đổi được m gam chất rắn. Kim loại M và giá trị m lần lượt là?
2. Hòa tan 8,1 gam bột kim loại X hóa trị III vào 2,5 lít dung dịch HNO3 0,5M (D=12,5 g/ml). Sau khi phản ứng kết thúc thu được 2,8 lít khí (đktc) hỗn hợp NO và N2. Biết tỉ khối của hỗn hợp khí trên so với heli là 7,2. Kim loại X và nồng độ phần trăm của dung dịch HNO3 lần lượt là?


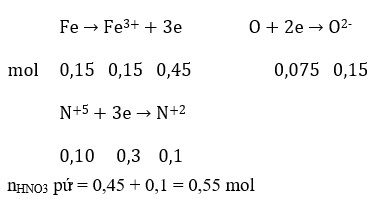

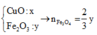
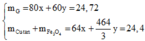

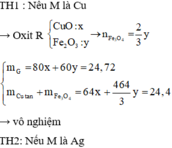
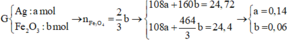


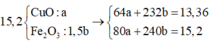
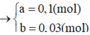



1) Gọi x là hóa trị cao nhất của M
\(n_{NO}=\frac{4,48}{22,4}=0,2\left(mol\right)\); \(n_M=\frac{19,2}{M_M}\left(mol\right)\)
Có: \(M^0-xe\rightarrow M^{+x}\)
__ \(\frac{19,2}{M_M}\) --> \(\frac{19,2x}{M_M}\) -> \(\frac{19,2}{M_M}\)
=> Số mol e nhường: \(\frac{19,2x}{M_M}\)
Có: \(N^{+5}+3e\rightarrow N^{+2}\)
_________ 0,6 <--- 0,2
=> Số mol e nhận: 0,6
Áp dụng DDLBT e => \(\frac{19,2x}{M_M}=0,6=>M_M=32x\)
Xét x =1 => \(M_M=32\) k có
Xét x =2 => \(M_M=64=>\) M là Cu
Chất rắn cuối cùng thu được là CuO
=> \(m_{CuO}=\frac{19,2}{64}.80=24\left(g\right)\)
2) Gọi số mol NO và N2 lần lượt là a,b (mol)
Ta có: \(\left\{{}\begin{matrix}\frac{30a+28b}{a+b}=28,8\\a+b=0,125\end{matrix}\right.\) => \(\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,075\left(mol\right)\end{matrix}\right.\)
\(n_X=\frac{8,1}{M_X}\left(mol\right)\)
Có: \(X^0-3e\rightarrow X^{+3}\)
___ \(\frac{8,1}{M_X}\) -> \(\frac{24,3}{M_X}\)
Có: \(N^{+5}+3e\rightarrow N^{+2}\)
_________ 0,15 <- 0,05
\(2N^{+5}+10e\rightarrow N_2^0\)
_______ 0,75 <- 0,075
Áp dụng ĐLBT e => \(\frac{24,3}{M_X}=0,15+0,75\) => \(M_X=27\) => M là Al
\(m_{HNO_3}=0,5.2,5.63=78,75\left(mol\right)\)
m dd HNO3 = \(2500.12,5=31250\left(g\right)\)
=> C% = \(\frac{78,75}{31250}.100\%=0,252\%\)