Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
→ n P 2 O 6 = 0 , 2 → C % H 3 P O 4 = 98 . 0 , 2 . 2 + 500 . 0 , 098 500 + 28 , 4 . 100 % = 16 , 69 %

Đáp án C
Ta có: nP2O5= 0,1 mol; mH3PO4 ban đầu= 250.9,8/100=24,5 gam
P2O5+ 3H2O→ 2H3PO4
0,1 0,2 mol
Tổng khối lượng H3PO4 là: 0,2.98+ 24,5=44,1 gam
Khối lượng dung dịch là: 14,2+ 250=264,2 gam
![]()

\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,15 0 ,05 0,15
a)\(V=0,15\cdot22,4=3,36\left(l\right)\)
b)\(m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,7}{9,8}\cdot100=150\left(g\right)\)
c) \(m_{H_2}=0,15\cdot2=0,3\left(g\right)\)
\(m_{ddsau}=2,7+150-0,3=152,4\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0,05\cdot342=17,1\left(g\right)\)
\(\Rightarrow C\%=\dfrac{17,1}{152,4}\cdot100=11,22\%\)

Ta có: \(n_{Fe_2O_3}=\dfrac{9,6}{160}=0,06\left(mol\right)\)
a. PTHH: Fe2O3 + 3H2SO4 ---> Fe2(SO4)3 + 3H2O (1)
Theo PT(1): \(n_{H_2SO_4}=3.n_{Fe_2O_3}=3.0,06=0,18\left(mol\right)\)
=> \(m_{H_2SO_4}=0,18.98=17,64\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{17,64}{m_{dd_{H_2SO_4}}}.100\%=9,8\%\)
=> \(m_{dd_{H_2SO_4}}=180\left(g\right)\)
b. Ta có: \(m_{dd_{Fe_2\left(SO_4\right)_3}}=9,6+180=189,6\left(g\right)\)
Theo PT(1): \(n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,06\left(mol\right)\)
=> \(m_{Fe_2\left(SO_4\right)_3}=0,06.400=24\left(g\right)\)
=> \(C_{\%_{Fe_2\left(SO_4\right)_3}}=\dfrac{24}{189,6}.100\%=12,66\%\)
c. PTHH: Fe2(SO4)3 + 3BaCl2 ---> 3BaSO4↓ + 2FeCl3 (2)
Theo PT(2): \(n_{BaSO_4}=3.n_{Fe_2\left(SO_4\right)_3}=3.0,06=0,18\left(mol\right)\)
=> \(m_{BaSO_4}=0,18.233=41,94\left(g\right)\)
Theo PT(2): \(n_{BaCl_2}=n_{BaSO_4}=0,18\left(mol\right)\)
=> \(m_{BaCl_2}=0,18.208=37,44\left(g\right)\)
Ta có: \(C_{\%_{BaCl_2}}=\dfrac{37,44}{m_{dd_{BaCl_2}}}.100\%=10,4\%\)
=> \(m_{dd_{BaCl_2}}=360\left(g\right)\)
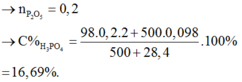


mk chỉ hd kiểu này nha
n P2O5=0.2m ; nH3PO4= 0.5 m (500/98*9.8%)
hòa tan P2O5 vào nc có pư: P2O5 + 3 H2O ----> 2H3PO4
___> tổng n H3PO4 = 0.5+0.4= 0.9m ====>88.2g
có mdd sau pư = m p205 + m h3po4 = 28.4 + 88.2 = 116.6g
=> C% h3po4 = (tự giải tiếp nha lười nghĩ :)))))
1 like nha mn
à nhầm chỗ m dd sau pư nha
phải là 28.4+500= 528.4 g chứ :)))