R có 2 loại đồng vị là R1 và R2. Tổng số hạt trong R1 là 54 hạt và trong R2 là 52 hạt. Biết R1 chiếm 25% và R2 chiếm 75%. Tính khối lượng nguyên tử trung bình của R?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1.Ta có: 2p+n1=54 ; 2p+n2=52
=>P=17=>n1=20=>n2=18
=>R=0,25∗37+0,75∗35=35,5
2
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 82:
p + e + n = 82 hay 2p + n = 82 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 22 hạt
(p+e) – n = 22 hay 2p – n = 22 (2)
Giải (1), (2) ta có p = e = 26; n =30
Số khối của X = Z + N = p + n =56
Bài 2:
a: Theo đề, ta có:
\(\left\{{}\begin{matrix}2Z+N=82\\Z-N=-4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3Z=78\\Z-N=-4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=26\\N=Z+4=30\end{matrix}\right.\)
A=26+30=56
b: Y: \(^{56}_{26}Fe\)

Đáp án C
Gọi số khối của X lần lượt là A1, A2, A3
Ta có hệ
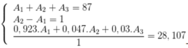
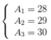
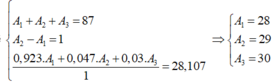
Gọi số p,n,e của R1 lần lượt là p1,n1,e1
=> 2p1+n1=54 => n1=54-2p1 (1)
Ta có BĐT : p1 \(\le n1\le1,5p1\)(2)
thay (1) vào (2) ta có :
p1 \(\le54-2p1\le1,5p1\)
=> 15,42\(\le p1\le18\)
=> p1=16,17,18
Với p1=16 => n1=22 => A=38 (loại)
p1=17 => n1=20 => A=37 => R : clo
p2= 18 => n1=18 => A=38 (loại)
Vậy AR1=38
Theo đề ta có : tổng số hạt trong đồng vị R1 lớn hơn tổng số hạt trong đồng vị R2 là 2 hạt mà số p,e trong 2 đồng vị ko đổi
=> nR1 - nR2 =2 (hạt)
=> AR1 - AR2=2 => AR2=35
=> \(\overline{M}=\dfrac{25\%.37+75\%.35}{100}=35,5\)(G/MOL)
Kết luận Ar1 phải là 37 chứ