3)Cho 13,92 gam hỗn hợp X gồm Cu và một oxit sắt vào dung dịch HNO3 loãng dư thu được 2,688 lít khí NO (sản phẩm khử duy nhất, đo ở đktc). Cô cạn dung dịch sau phản ứng thu được 42,72 gam muối khan. Công thức của oxit sắt là A. FeO. B. Fe3O4 C. Fe2O3 D. Fe3O4 hoặc FeO.
Bạn có để ý rằng nếu một hỗn hợp chứa các chất khử có lượng cho trước và độ tăng số oxi hóa không đổi sẽ phóng ra một lượng mol electron không đổi cho các chất oxi hóa.
Trở về bài toán, ta thấy X phóng ra lượng mol electron không đổi là 0,36mol (ĐLBT Electron)
Vậy, khi pứ với OO cũng sẽ phóng ra lượng mol electron trên => nOnO=0,18mol. =>mOmO=2,88.
Ta thấy rằng mX+mO=mFe2O3+mCuOmX+mO=mFe2O3+mCuO => mFe2O3+mCuOmFe2O3+mCuO=16,8g.
Ta gọi x là nFe2O3nFe2O3, y là nCuOnCuO.
=> 160x+80y=16,8 (I)
Từ khối lượng Muối => 484x+126y=42,72 (II)
=>x=0,03 . y=0,15
Ta có nOnO trong oxit sắt ban đầu = nO(Fe2O3)nO(Fe2O3)-nOnO pứ với oxit sắt ban đầu (0,18-nOnO(CuO)(CuO))
==> nOnO trong oxit sắt ban đầu = 0,03.3 - 0,03=0,06 mol.
Ta có nFenFe=0,06. nOnO=0,06 => FeOFeO.



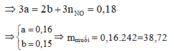
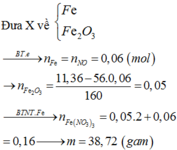
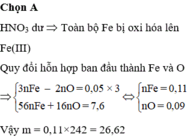

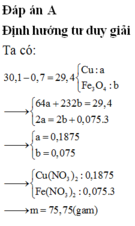
khó quá mik ko bt
kho qua ko hieu