hòa tan 1 lượng hidroxit kim loại có hóa trị n trong đ H2SO4 vừa đủ thu được 1 lượn muối có khối lượng gấp 1,724 lần khối lượng hidroxit đem hòa tan. Xác định CT của hidroxit ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi kim loại cần tìm là R(OH)2
PTHH: \(R\left(OH\right)_2+H_2SO_4\rightarrow RSO_4+2H_2O\)
Đặt số mol hidroxit phản ứng là 1 mol
=> \(m_{ddH_2SO_4}=\dfrac{1.98}{17,98\%}=545\left(g\right)\)
=> \(m_{ddsaupu}=M+34+545=M+579\left(g\right)\)
Ta có : \(C\%_{MSO_4}=\dfrac{M+96}{M+579}.100=25\%\)
=> M=65 (Zn)

Đáp án A.
Coi nH2SO4 = 1 mol
M(OH)2 + H2SO4 → MSO4 + 2H2O
mdd H2SO4= 1.98.100/20 = 490 (gam)
=> mdd sau = (M + 34) + 490 = M + 524


M(OH)2 + H2SO4 ----->MSO4 + 2H2O
1---------------1-----------------1
Coi ban đầu có 1 mol H2SO4>>mH2SO4 = 98
>>mdd H2SO4 = 98/20*100 = 490
mdd sau phản ứng =(M+17*2)+490=M + 524
Vì MSO4 có nồng độ bằng 27,21& nên
(M+96)/(M+524) = 0.2721
>>M = 64 (Cu)

PTHH: MCl2 + 2AgNO3 → M(NO3)2 + 2AgCl ↓
Theo pt: Số mol MCl2 = Số mol M(NO3)2
Mà: Khối lượng mol của MCl2 < Khối lượng mol của M(NO3)2 => Khối lượng muối M(NO3)2 hơn khối lượng muối ban đầu là 1,59(gam).
Khối lượng muối M(NO3)2 sau phản ứng là:
3,33 + 1,59 = 4,92 (gam)
Số mol MCl2 tính theo khối lượng là:
3,33 / MM + 71
Số mol M(NO3)2 tính theo khối lượng là:
4,92 / MM + 124
Mà: Số mol của 2 muối là bằng nhau
=> 3,33 / MM + 71 = 4,92 / MM + 124
=> MM = 40 ( Canxi )
=> Công thức hoá học của muối Clorua kim loại M là: CaCl2

Xét 1 mol kim loại ứng với R (gam) tham gia phản ứng.
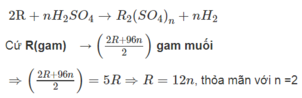
Vậy R=24 (Mg)

Đáp án D
Khi hòa tan 1 mol kim loại R thì thu được 0,5 mol R2(SO4)n (khi n = 2 thì thu được 1 mol RSO4, có thể coi là 0,5 mol R2(S04)2)
0,5.(2R + 96n) = 5R Û R = 12n Þ n = 12, R = 24 là Mg.