Tổng số hạt proton, nơtron, electron của nguyên tử của một nguyên tố thuộc nhóm VIIA là 28.
a) Tính nguyên tử khối.
b) Viết cấu hình electron nguyên tử của nguyên tố đó.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nguyên tố cần tìm thuộc nhóm VIIA → nguyên tử có 7e ở lớp ngoài cùng. Vì lớp thứ nhất chỉ chứa tối đa 2e nên nguyên tử của nguyên tố này phải có ít nhất 2 lớp electron (n ≥ 2).
+ Nếu n = 2, có 2 lớp e, số e ở các lớp là : 2,7 → nguyên tử gồm : 9p, 9e và 10n (tổng số hạt là 28, phù hợp đề bài).
+ Nếu n = 3, có 3 lớp e, số e ờ các lớp là : 2, 8, 7 → vậy chỉ riêng số p + số e = 17 + 17 = 34 > 28 → trái với đề bài. Vậy nguyên tố cần tìm có z = 9 với cấu hình electron : 1 s 2 2 s 2 2 p 5

Nguyên tố cần tìm thuộc nhóm VIIA → nguyên tử có 7e ở lớp ngoài cùng. Vì lớp thứ nhất chỉ chứa tối đa 2e nên nguyên tử của nguyên tố này phải có ít nhất 2 lớp electron (n ≥ 2).
+ Nếu n = 2, có 2 lớp e, số e ở các lớp là : 2,7 → nguyên tử gồm : 9p, 9e và 10n (tổng số hạt là 28, phù hợp đề bài).
+ Nếu n = 3, có 3 lớp e, số e ờ các lớp là : 2, 8, 7 → vậy chỉ riêng số p + số e = 17 + 17 = 34 > 28 → trái với đề bài. Vậy nguyên tố cần tìm có z = 9 với cấu hình electron : 1 s 2 2 s 2 2 p 5

Nguyên tố thuộc nhóm VIIA nên có 7e lớp ngoài cùng:
Cấu hình electron: 1s22s22p5.

Tính nguyên tử khối.
Gọi tổng số hạt p là Z, tổng số hạt n là N, tổng số hạt e là E, ta có: Z + N + E = 28
Vì Z = E nên suy ra: 2Z + N = 28.(1)
Các nguyên tử có Z < 83. Mặt khác
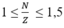
→ Z ≤ N ≤ 1,5Z
Từ (1) ⇒ Z < 28 - 2Z < 1,5Z
⇔ 3Z ≤ 28 ≤ 3,5Z → 8 ≤ Z ≤ 9,33
Z nguyên dương nên chọn Z = 8 và 9.
A = Z + N
| Z | 8 | 9 |
| N | 12 | 10 |
Nếu Z = 8 → A = 20 (loại vì nguyên tố có Z = 8 thì A = 16).
Nếu Z = 9 → A = 19 chấp nhận vì nguyên tố có Z = 9 thì A = 19.

Đáp án A
R thuộc nhóm VIIA, hợp chất với hidro có dạng RH
Tổng số hạt bằng 28: 2p + n = 28, p < 14 => R là F.

Chọn A
R thuộc nhóm VIIA → Loại C và D.
Tổng số hạt trong nguyên tử R là 28 → loại B.

- Trong nguyên tử thì tỉ số N/Z ≥ 1 và N/Z ≤ 1,5
- Trong nguyên tử số proton bằng số electron.
Theo đầu bài tổng 3 loại hạt là 13. Ta có thể biện luận như sau :
+ Nếu số p = số e = 3 thì số n = 13 - (3 + 3) = 7.
Tỉ số N/Z = 7/3 = 2,3 > 1,5 (loại)
+ Nếu số p = số e = 4 thì số n = 13 - (4 + 4) = 5.
Tỉ số N/Z = 5/4 = 1,25 (phù hợp)
+ Nếu số p = số e = 5 thì số n = 13 - (5 + 5) = 3.
Tỉ số N/Z = 3/5 = 0,6 < 1 (loại)
Vậy nguyên tử đó có Z = 4. Đó là beri (Be).
Nguyên tử khối của nguyên tố đó là : 4 + 5 = 9 đvC.
Cấu hình electron nguyên tử : 1 s 2 2 s 2
a) Tính nguyên tử khối.
Gọi tổng số hạt p là Z, tổng số hạt n là N, tổng số hạt e là E, ta có:
Z + N + E = 28.
Vì Z = E, nên suy ra 2Z + N = 28
Các nguyên tử có Z < 83 thì
1 ≤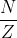 ≤ 1,5 → Z ≤ N ≤ 1,5Z
≤ 1,5 → Z ≤ N ≤ 1,5Z
2Z + Z < N + 28 - N < 1,5N + 2Z
3Z ≤ 28 ≤ 3,5Z → 8 ≤ Z ≤ 9,33.
Z nguyên dương nên chọn Z = 9 và 9
A = Z + N
Z = 8 → N = 12
Z = 9 → N = 10
Nếu Z = 8 → A = 20 (loại vì nguyên tố có Z = 8 thì A = 16)
Nếu Z = 9 → A = 19 (chấp nhận vì nguyên tố có Z = 9 thì A = 19
b) Nguyên tố thuộc nhóm VIIA nên có 7e lớp ngoài cùng:
Cấu hình electron: 1s22s22p5.
bạn viết kĩ chỗ biến đổi ra được k