đốt cháy hoàn toàn 19,2g kim loại X có hóa trị 2 cần dùng hết 8,96l oxi ở đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số mol của khí oxi ở dktc
nO2 = \(\dfrac{V_{O2}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : 2X + O2 → 2XO\(|\)
2 1 2
0,4 0,2
Số mol của kim loại X
nX = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ MX = \(\dfrac{m_X}{n_X}=\dfrac{22,4}{0,4}=56\) (dvc)
Vậy kim loại x là Fe
Chúc bạn học tốt

PTHH: \(4R+xO_2\xrightarrow[]{t^o}2R_2O_x\) (x là hóa trị của kim loại R)
Ta có: \(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow n_R=\dfrac{0,4}{x}\left(mol\right)\) \(\Rightarrow M_R=\dfrac{13}{\dfrac{0,4}{x}}=\dfrac{65x}{2}\)
Ta thấy với \(x=2\) thì \(M_R=65\)
Vậy kim loại cần tìm là Kẽm (Zn)

nO2 = 8,4/22,4 = 0,375 (mol)
PTHH: 4X + 5O2 -> (t°) 2X2O5
Mol: 0,3 <--- 0,375
M(X) = 9,3/0,3 = 31 (g/mol)
=> X là P

4Al+3O2-to>2Al2O3
0,04---0,03------0,02 mol
n Al=\(\dfrac{1,08}{27}\)=0,04 mol
=>VO2=0,03.22,4=0,672l
b)
2A+O2-to>2AO
0,06--0,03 mol
=>\(\dfrac{3,84}{A}=0,06\)
=>A=64 :=>Al là Đồng

\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2A+O_2\rightarrow\left(t^o\right)2AO\)
0,4 0,2 ( mol )
\(M_A=\dfrac{4,8}{0,4}=12\) ( g/mol )
--> A là Cabon ( C )

\(n_{O_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: 4M + nO2 --to--> 2M2On
\(\dfrac{0,12}{n}\leftarrow0,03\)
\(\Rightarrow M_M=\dfrac{1,08}{\dfrac{0,12}{n}}=9n\left(\dfrac{g}{mol}\right)\)
Xét n = 3 tm => MM = 27 (g/mol)
=> M là Al
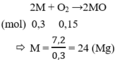
\(X+\dfrac{1}{2}O_2-^{t^o}\rightarrow XO\)
\(n_X=2n_{O_2}=0,8\left(mol\right)\)
=> \(M_X=\dfrac{19,2}{0,8}=24\left(Mg\right)\)
PTHH: \(2X+O_2\xrightarrow[]{t^o}2XO\)
Ta có: \(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow n_X=0,8\left(mol\right)\) \(\Rightarrow M_X=\dfrac{19,2}{0,8}=24\) (Magie)