cho 3,2 g cuo tác dụng vừa đủ với dung dịch H2SO4 , 4,9%. Tính nồng độ phần trăm của dung dịch CuSO4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nCuO=3,2:80=0,04 mol
PTHH: CuO+H2SO4=>CuSO4+H2O
0,04mol->0,04mol->0,04mol->0,04mol
=> m H2SO4=0,04.98=3,92g
=> m ddH2SO4 tham gia phản ứng =\(\frac{3,92.100}{4,9}=80\)g
theo địnhluật bảo toàn khối lượng => m CuSO4= mCuO+mH2SO4-mH2O=3,2+80-0,04.18=82,48g
m CuSO4 thu được= 0,04.160=6,4g
=> C% CuSO4 =\(\frac{6,4}{82,48}.100=7,76\%\)
:)

a) \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
b) \(n_{CuO}=\dfrac{3,2}{80}=0,04\left(mol\right)=n_{H_2SO_4}=n_{CuSO_4}\)
\(m_{ddH_2SO_4}=\dfrac{0,04.98}{4,9\%}=80\%\)
\(m_{ddsaupu}=3,2+80=83,2\left(g\right)\)
=> \(C\%_{CuSO_4}=\dfrac{0,04.160}{83,2}.100=7,69\%\)

(Đề bài thiếu dữ kiện để tính khối lượng dung dịch)
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
$n_{CuSO_4} = n_{CuO} = \dfrac{8}{80} = 0,1(mol)$
$m_{CuSO_4} = 0,1.160 = 16(gam)$
Sau phản ứng :
$m_{dd} = m_{CuO} + m_{dd\ H_2SO_4} = 8 + m_{dd\ H_2SO_4}(gam)$
Suy ra :
$C\%_{CuSO_4} = \dfrac{16}{8 + m_{dd\ H_2SO_4}}.100\%$

\(n_{CuO}=\dfrac{3,2}{80}=0,04\left(mol\right)\\
pthh:CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
0,04 0,04 0,04 0,04
\(m_{\text{dd}_{H_2SO_4}}=\dfrac{\left(0,04.36,5\right).100}{4,9}=29,79\left(g\right)\\
m_{\text{dd}_{CuSO_4}}=3,2+29,79-\left(0,04.2\right)=32,91\left(g\right)\\
C\%_{\text{dd}}=\dfrac{0,04.160}{32,91}.100\%=19,44\%\)

nCuO=16/80=0,2(mol)
a) PTHH: CuO + H2SO4 -> CuSO4 + H2O
0,2___________0,2_____0,2(mol)
b) mCuSO4=160.0,2=32(g)
c) mH2SO4=0,2.98=19,6(g)
=>C%ddH2SO4= (19,6/100).100=19,6%
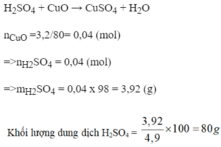

nCuO=0,04 mol
CuO + H2SO4 =>CuSO4 + H2O
0,04 mol=>0,04 mol=>0,04 mol
mH2SO4=0,04.98=3,92 gam
=>m dd H2SO4=3,92/4,9%=80 gam
mCuSO4 sau=0,04.160=6,4 gam
mdd CuSO4=3,2+80=83,2 gam
C% dd CuSO4=6,4/83,2.100%=7,69%
cho \(m_{CuO}=3,2g\Rightarrow n_{CuO}=\frac{3,2}{80}=0,04mol\)
PTHH:
CuO + H2SO4 -> CuSO4 + H2O
0,04mol----------->0,04mol--------->0,04mol
ta có: \(m_{H_2SO_4}=0,04.98=3,92g\)
\(C\%_{d^2H_2SO_{4_{ }}}=4,9\%\)
=. \(m_{d^2H_2SO_4}=\frac{m_{H_2SO_4}.100}{C\%}=\frac{3,92.100}{4,9}=80g\)
áp dụng ĐLBTKL ta có: \(m_{d^2CUSO_4}=m_{CuO}+m_{d^2H_2SO_4}=3,2+80=83,2g\)
\(m_{CuSO_4}=0,04.160=6,4g\)
\(\Rightarrow C\%_{d^2CuSO_4}=\frac{m_{CuSO_4}}{m_{d^2CuSO_4}}.100=\frac{6,4}{83,2}.100=7,69\%\)