Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(nNa_2CO_3=\dfrac{10,6}{106}=0,1\left(mol\right)\)
Vdd = 200 ml = 0,2(l)
\(Na_2CO_3+H_2O\rightarrow NaHCO_3+NaOH\)
1 1 1 1 (mol)
0,1 0,1 0,1 0,1 (mol)
theo đề ta suy ra : mdd = 1,05 . 200 = 210 (g)
\(mNaHCO_3=0,1.84=8,4\left(g\right)\)
\(mNaOH=0,1.40=4\left(g\right)\)
=> ndd sau pứ = 0,1 + 0,1 = 0,2 (mol)
m dd vừa đc pha chế = m NaHCO3 + mNaOH
= > mdd vừa đc pha chế = \(8,4+4=12,4\left(g\right)\)
\(C\%dd=\dfrac{12,4.100}{210}=5,9\%\)
\(CM_{dd}=\dfrac{n_{dd}}{V_{dd}}=\dfrac{0,2}{0,2}=1M\)

VNaOH = 200ml = 0,2 (l)
CuCl2 + 2NaOH ---> Cu(OH)2 + 2NaCl
Kết tủa là Cu(OH)2
=> mCu(OH)2 = 9,8 / 98 = 0,1 (mol)
=> nNaOH = 0,2 (mol)
=> CM NaOH = n/V = 0,2 / 0,2 = 1M

Nồng độ % của dung dịch Na2CO3.
Mdd = V.d = 200 x 1,05 = 210g dung dịch Na2CO3.
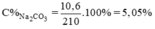
Nồng độ mol/l của dung dịch.
200ml = 0,2l.
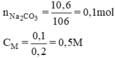

1ml dung dịch cho khối lượng 1,05 gam
200 ml dung dịch cho khối lượng m dd = 210 gam
Nồng độ phần trăm:
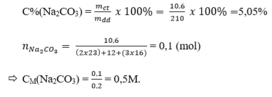

1ml dung dịch cho khối lượng 1,05 gam
200 ml dung dịch cho khối lượng mdd = 210 gam
Nồng độ phần trăm:
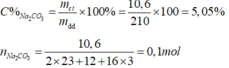
C M Na 2 CO 3 = 0 , 1 : 0 , 2 = 0 , 5 M .

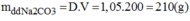
Nồng độ phần trăm của dung dịch pha chế:
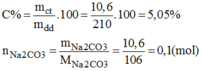
Nồng độ mol của dung dịch:
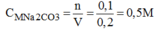

PTHH:
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
mKL tăng : \(mAg-mCu=29,12-20=9,12g\)
=>\(nCu=\dfrac{9,12}{108.2-64}=0,06mol\)
\(nAgNO_3=0,3.0,5=0,15mol\)
tỉ lệ so sánh :
\(\dfrac{nAgNO_3}{2}>\dfrac{nCu}{1}\left(0,075>0,06\right)\Leftrightarrow nAgNO_{3\left(dư\right)}=0,15-0,06.2=0,03mol\)
thep pt: \(nCu\left(NO_3\right)_2=nCu=0,06mol\)
\(\Leftrightarrow C_{MCu\left(NO_3\right)_2}=\dfrac{0,06}{0,5}=0,12M\)
\(C_{MAgNO_{3\left(dư\right)}}=\dfrac{0,03}{0,5}=0,06M\)
vậy nồng độ mol chất Cu(NO3)2 và AgNO3(dư) lần lượt là 0,12M và 0,06M