Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

sao chị ko đáp lại câu trả lời của em ở câu trước , chị ko biết hả ?

Đáp án D
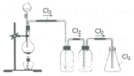
Để loại bỏ tạp chất người ta dẫn khí clo lần lượt qua các bình:
Bình đựng dung dịch NaCl bão hòa để loại khí hiđro clorua (HCl)
Bình đựng H2SO4 đặc để loại bỏ hơi nước.

a)
Giả sử lấy lượng mỗi chất là a gam.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (1)
2KMnO4 + 14 HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O (2)
K2Cr2O7 + 14 HCl → 2CrCl2 + 2KCl + 3Cl2 + 7H2O (3)
Vậy dùng : KMnO4 điều chế được nhiều Cl2 hơn
b) Nếu số mol các chất bằng n mol
Theo (1) nmol MnO2 → nmol Cl2
Theo (2) nmol KMnO4 → 2,5 nmol Cl2
Theo (3) nmol K2Cr2O7 → 3nmol Cl2
Ta có: 3n > 2,5n > n
Vậy dùng K2Cr2O7 được nhiều hơn Cl2 hơn
a) Giả sử lấy lượng mỗi chất là a gam.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (1)
2KMnO4 + 14 HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O (2)
K2Cr2O7 + 14 HCl → 2CrCl2 + 2KCl + 3Cl2 + 7H2O (3)
Vậy dùng : KMnO4 điều chế được nhiều Cl2 hơn
b) Nếu số mol các chất bằng n mol
Theo (1) nmol MnO2 → nmol Cl2
Theo (2) nmol KMnO4 → 2,5 nmol Cl2
Theo (3) nmol K2Cr2O7 → 3nmol Cl2
Ta có: 3n > 2,5n > n
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn

thí nghiệm chi cái giờ bắt học sinh tính mắc mệt:( ai giúp em zới
PTHH:
Fe3O4 + 4CO -> (t°) 3Fe + 4CO2
0,2 ---> 0,8 ---> 0,6 ---> 0,8
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
0,2 ---> 0,6 ---> 0,4 ---> 0,6
VCO = 0,8 . 22,4 = 17,92 (l)
VH2 = 0,6 . 22,4 = 13,44 (l)
nFe = 0,4 + 0,6 = 1 (mol)
mFe = 1 . 56 = 56 (g)

Câu 8:
\(n_{Cl_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,1<---------------------------------0,25
=> \(n_{KMnO_4\left(tt\right)}=\dfrac{0,1.100}{80}=0,125\left(mol\right)\)
=> mKMnO4(tt) = 0,125.158 = 19,75 (g)
Câu 18:
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> n2 muối cacbonat = 0,1 (mol)
Câu 8: 2KMnO4 (0,125 mol) + 16HCl (đậm đặc) \(\underrightarrow{H=80\%}\) 2KCl + 2MnCl2 + 5Cl2\(\uparrow\) (0,25 mol) + 8H2O.
Khối lượng thuốc tím cần dùng là 0,125.158=19,75 (g).
Câu 18: 2H+ + CO32- (0,1 mol) \(\rightarrow\) CO2 (0,1 mol) + H2O.
Số mol của hỗn hợp hai muối cacbonat là 0,1 mol.

số mol kẽm tham gia phản ứng là:\(n_{Zn}=\frac{m}{M}=\frac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 (mol)
a, thể tích khí hiđro thu được là:\(V_{H_2}=n_{H_2}\times22,4=0,1\times22,4=2,24\left(l\right)\)
b,khối lượng HCl cần dùng là:\(m_{HCl}=n_{HCl}\times M=0,2\times65=13\left(g\right)\)

Đáp án C