Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

(1) 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
(2) Fe2O3 + 6HCl → 2FeCl3 + 3H2O
(3) FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
(4) 2Fe(OH)3 → Fe2O3 + 3H2O.
(5) FeO + H2SO4 → FeSO4 + H2O.
(6) FeSO4 + Mg → MgSO4 + Fe.

Đáp án B
• Xét tại thời điểm th; dung dịch sau điện phân hòa tan Al sinh ra H2 mà tỷ lệ CuSO4 : NaCl = 1:1 nên.
Đặt số mol CuSO4 và NaCl đều là b mol.
Ở catot: Cu2+ + 2e → Cu0; ở anot: 2Cl- - 2e → Cl2 ; 2H2O – 4e → 4H+ + O2.
Dung dịch X Phản ứng với Al sinh ra a mol H2 → lượng H+ đã phản ứng = 2a mol.
||→ Số mol e trao đổi = b + 2a mol .
• Xét tại thời điểm 2th, số mol e trao đổi = 2 (2a + b) mol.
Ở catot: Cu2+ + 2e → Cu0 ; 2H2O + 2e → 2OH- + H2 || Ở anot: 2Cl- - 2e → Cl2 ; 2H2O – 4e → 4H+ + O2.
Số mol e Cl- nhường = b mol → số mol e H2O nhường = 4a + b mol → Lượng H+ sinh ra = 4a + b
Số mol e Cu2+ nhận = 2b mol → Số mol e H2O nhận = 4a mol → số mol OH- = 4a mol.
Trong dung dịch có OH- và H+ nên : H+ + OH- → H2O.
||→ Lượng H+ dư = b mol.
Cho Al dư vào dung dịch: Al + 3H+ → Al3+ + 3/2 H2.
||→ Số mol H2 = b /2 = 4a → a : b = 1 : 8
• Xét các nhận định:
+ Tại thời điểm 2th số mol khí thoát ra ở hai cực là: 2a + 0,5 b + 0,25 (4a + b ) , thay b = 8 a → số mol khí thoát ra = 9a mol → (1) đúng.
+ Tại thời điểm 1,75t h thì số mol e trao đổi = 1,75 (2a + b) mol.
Nếu H2O điện phân thì Cu2+ điện phân hết → số mol e Cu2+ nhận = 2b mol < 1,75 (2a + b)
||→ 0,25b < 3,5a → a : b < 1 / 3 đúng (do a : b = 0,75). → (2) đúng.
+ Tại thời điểm 1,5t h thì số mol e trao đổi = 1,5 (2a + b) mol.
Nếu H2O điện phân thì Cu2+ điện phân hết → số mol e Cu2+ nhận = 2b mol < 1,5 (2a + b)
||→ 0,5b < 3a → a : b < 1 / 6 → đúng (do a : b = 1:8 ). → (3) đúng.
+ Tại thời điểm 0,8t h thì số mol e trao đổi = 0,8 (2a + b) mol.
Nếu H2O điện phân thì Cl- điện phân hết → số mol e Cl- nhường= b mol < 0,8 (2a + b)
||→ 0,2b < 1,6 a → a : b < 1 / 8 đúng (do a : b = 1:8). → (4) đúng.
+ Tại thời điểm 2th thì số mol H2 sinh ra = 2a mol. → (5) sai.

Chọn B.
Tại thời điểm t (s) có khí Cl2 (0,06 mol) Þ ne (1) = 0,12 mol
Tại thời điểm 2t (s) có 2 khí Cl2 (x mol) và O2 (y mol) Þ
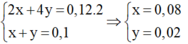
Tại thời điểm 4t (s) có 3 khí H2 (a mol); Cl2 (0,08 mol) và O2 (b mol) Þ ne (4) = 0,48 mol
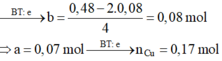
Tại thời điểm 3t (s) Þ ne (3) = 0,36 mol có C u : 0 , 17 m o l C l 2 : 0 , 08 m o l
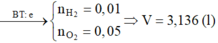

k = 2
- A, B, D không phản ứng với Na =>A, B, D không có H linh động
- A + NaOH → 1 muối + 2 ancol kế tiếp nhau trong cùng 1 dãy đồng đẳng. Vậy A là este của axit 2 chức no và 2 ancol no đơn chức đồng đẳng kế tiếp.
→ CTCT của A: CH3OOC-CH2-COO-C2H5
- B + NaOH →2 muối + 1ancol => B là este của ancol 2 chức no và 2 axit đơn chức no
→ CTCT của B: HCOO-CH2-CH2-CH2-OOCCH3 hoặc HCOO-CH2-CH2-OOC-CH2-CH3
- D + NaOH → 1 muối + 1 ancol => D là este của 1 axit no 2 chức và 1 ancol no đơn chức hoặc 1 axit no đơn chức và 1 ancol no hai chức.
→ Vậy D có thể có các CTCT sau:
CH3-OOC-CH2-CH2-COOCH3 ; C2H5-OOC-COO-C2H5 ; CH3-COO-CH2-CH2-OOC-CH3, HCOO-CH2-CH2-CH2-CH2-OOCH
Đáp án cần chọn là: B

Đáp án B
- Đặt số mol của Cu(NO3)3 và NaCl là x và y
- Phương trình điện phân:
Tại catot:
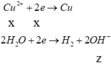
Tại anot
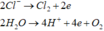
- Điện phân t(s):
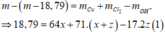
- Điện phân 2t(s): hỗn hợp khí T chứa 3 khí
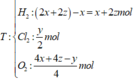
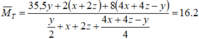
![]()
a gam dung dịch Z:
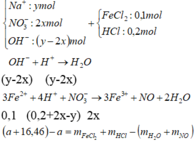
Dung dịch sau phản ứng không chứa H+
=> H + phản ứng hết
16 , 46 = 127 , 01 + 36 , 5 . 0 , 2 - 18 . y - 2 x + 0 , 2 + 2 x - y 2 - 30 . 0 , 2 - 2 x - y 4 ( 3 )
Từ (1), (2), (3) suy ra:
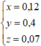
=> m=188x + 58,5y = 45,96 g
a = 62.2x + 23y + 17.(y-2x) = 26,8 => a + m = 72,76 g
