Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nhh = 0,1 mol.
Giả sư: nC2H4 = nC3H6 = a mol → nH2 = 1 - 2a mol.
→ mX = 28a + 42a + 2(0,1 - 2a) = 15,2 x 0,1
→ a = 0,02 mol.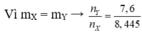
→ nY = 0,09 mol.
Ta có nH2phản ứng = nX - nY = 0,1 - 0,09 = 0,01 mol.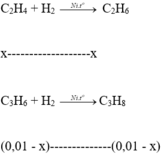
mbình tăng = (0,02 - x) x 28 + (0,02 - 0,01 + x) x 42 = 1,015
→ x = 0,0025 mol.

Đáp án C
Hướng dẫn
mX = 18,5.1 = 18,5 g; nY = 18,5/20 = 0,925 mol => nH2 pư = 1 – 0,925 = 0,075 mol

Đáp án C
Bảo toàn khối lượng: mY = mX = 1 × 9,25 × 2 = 18,5(g)
⇒ nY = 18,5 ÷ (10 × 2) = 0,925 mol.
||⇒ nH2 phản ứng = ∆n = nX – nY = 1 – 0,925 = 0,075 mol

Đáp án B
Ta có C2H4 + H2 → C2H6
C3H6 + H2 → C3H8
nX = 1 mol
Bảo toàn khối lượng có mY = mX = 1.9,25.2 =18,5 → nY =
→nH2 = nX – nY = 0,075 mol

Đáp án C
TQ : CnH2n + H2 -> CnH2n+2
Vì đun nóng trong bình kín nên mX = mY = nX.MX = 1.2.9,25 = 18,5g
=> nY = 0,925 mol
=> nX – nY = nH2 pứ = 1 – 0,925 = 0,075 mol

Đáp án B
Áp dụng phương pháp đường chéo cho hỗn hợp X:
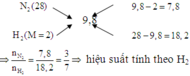
Cách 1: Gọi số mol N2 là 3x thì số mol H2 là 7x ⇒ tổng số mol hỗn hợp X là 3x + 7x = 10x
Thay vào công thức:
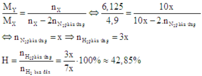
Cách 2: Áp dụng công thức tính nhanh với trường hợp x < 3y:
Hiệu suất phản ứng:
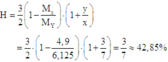
Đáp án D
Giả sử ban đầu có 40 mol khí, sau phản ứng sẽ có 31 mol khí.
Sử dụng đường chéo, ta tính được
Do sau phản ứng vẫn thu được hỗn hợp khí nên H2 sẽ dư
Số mol H2 phản ứng: 40-31=9
Hiệu suất phản ứng: H= 9 16 = 56 , 25 %