Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

V1:V1: Thể tích H2SO4 1 M
V2:V2: Thể tích H2SO4 2 M
VH2SO4=V1+V2=0.05(l)(1)VH2SO4=V1+V2=0.05(l)(1)
nH2SO4=V1+2V2=0.05⋅1.5=0.075(mol)(2)nH2SO4=V1+2V2=0.05⋅1.5=0.075(mol)(2)
(1),(2):V1=0.025,V2=0.025(1),(2):V1=0.025,V2=0.025
Đong lấy 25 ml dung dịch H2SO4 1M và 25 ml dung dịch H2SO4 2M cho vào bình tam giác, lắc đều, ta được 50 ml dung dịch H2SO4 1,5M.

Pha chế 50ml dung dịch H 2 S O 4 1,5M.
- Số mol H 2 S O 4 cần pha chế 50ml dung dịch H 2 S O 4 1,5M:
n H 2 S O 4 = CM.V = 1,5.0,05 = 0,075 (mol)
Gọi x(ml) là thể tích của dung dịch H 2 S O 4 1M (1)
Gọi y(ml) là thể tích của dung dịch H 2 S O 4 3M (2)
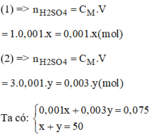
Giải hệ phương trình ta có: x = 37,5ml; y = 12,5ml
- Cách pha chế:
+ Đong lấy 37,5ml dung dịch H 2 S O 4 1M và 12,5ml dung dịch H 2 S O 4 3M cho vào bình, lắc đều, ta được 50ml dung dịch H 2 S O 4 1,5M.

\(V_1:\) Thể tích H2SO4 1 M
\(V_2:\) Thể tích H2SO4 2 M
\(V_{H_2SO_4}=V_1+V_2=0.05\left(l\right)\left(1\right)\)
\(n_{H_2SO_4}=V_1+2V_2=0.05\cdot1.5=0.075\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):V_1=0.025,V_2=0.025\)
Đong lấy 25 ml dung dịch H2SO4 1M và 25 ml dung dịch H2SO4 2M cho vào bình tam giác, lắc đều, ta được 50 ml dung dịch H2SO4 1,5M.

* Số mol của H 2 S O 4 cần để pha chế 500ml dung dịch H 2 S O 4 1M:
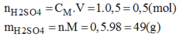
* Khối lượng H 2 S O 4 98% có chứa 49g H 2 S O 4 :
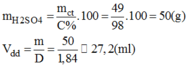
* Cách pha chế: Đổ khoảng 400ml nước cất vào cốc có chia độ có dung tích khoảng 1lit. Rót từ từ 27,2ml H 2 S O 4 98% vào cốc khuấy đều. Sau đó thêm dần dần nước cất vào cốc cho đủ 500ml. ta pha chế được 500ml dung dịch H 2 S O 4 1M.

Bài 1:
Ta có: \(n_{H_2SO_4}=0,05.2=0,1\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,1.98=9,8\left(g\right)\)
Bài 2:
Ta có: n đường (1) = 2.0,5 = 1 (mol)
n đường (2) = 3.1 = 3 (mol)
⇒ Σn đường = 1 + 3 = 4 (mol)
\(\Rightarrow C_M=\dfrac{4}{2+3}=0,8M\)
Bài 3:
_ Tính toán:
Ta có: \(n_{CuSO_4}=0,075.2=0,15\left(mol\right)\)
\(\Rightarrow m_{CuSO_4}=0,15.160=24\left(g\right)\)
_ Cách pha chế: Cân lấy 24 gam CuSO4 cho vào cốc thủy tinh dung tích 100 ml. Đổ dần dần nước cất vào cốc và khuấy nhẹ cho đủ 75 ml dung dịch. Ta được 75 ml dung dịch CuSO4 2M.
Bài 4:
_ Tính toán:
Ta có: \(m_{CuSO_4}=150.7\%=10,5\left(g\right)\)
⇒ mH2O = 150 - 10,5 = 139,5 (g)
_ Cách pha chế: Cân lấy 10,5 gam CuSO4 cho vào cốc có dung tích 200 ml. Cân lấy 139,5 gam (hoặc đong lấy 139,5 ml) nước cất rồi đổ dần vào cốc và khuấy nhẹ, ta được 150 gam dung dịch CuSO4 7%.
Bạn tham khảo nhé!

\(n_{K_2SO_4}=0,4.0,5=0,2\left(mol\right)\\ n_{KOH}=0,25.0,4=0,1\left(mol\right)\)
PTHH: 2KOH + H2SO4 ---> K2SO4 + 2H2O
0,4 0,2 0,2
\(\rightarrow\left\{{}\begin{matrix}V_{KOH}=\dfrac{0,4+0,1}{2}=0,25\left(l\right)=250\left(ml\right)\\V_{H_2SO_4}=\dfrac{0,2}{2,5}=0,08\left(l\right)=80\left(ml\right)\end{matrix}\right.\\ \rightarrow V_{H_2O}=400-250-80=70\left(ml\right)\)
PP: hoà 250 ml dd KOH 2,5M vào 80 ml dd H2SO4 80 ml sau đó thêm 70 ml nước cất ta được dd ...

Gọi VddH2SO4 (2M) = a (l)
=> nH2SO4 (2M) = a (mol)
Gọi VddH2SO4 (1M) = b (l)
=> nH2SO4 (1M) = 2b (mol)
nH2SO4 (1,5M) = 0,05 . 1,5 = 0,075 (mol)
Ta có:
a + b = 0,05 (l)
a + 2b = 0,075 (mol)
=> a = b = 0,025 (l)
=> VddH2SO4 (1M) = VddH2SO4 (2M) = 0,025 (l)
V1: Thể tích H2SO4 1 M
V2: Thể tích H2SO4 2 M
VH2SO4=V1+V2=0.05(l)(1)
nH2SO4=V1+2V2=0.05⋅1.5=0.075(mol)(2)
(1),(2):V1=0.025,V2=0.025
Đong lấy 25 ml dung dịch H2SO4 1M và 25 ml dung dịch H2SO4 2M cho vào bình tam giác, lắc đều, ta được 50 ml dung dịch H2SO4 1,5M.