Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CTHH của oxit sắt là Fe2Oy (y > 0)
Theo bài ra,ta có:
56.2 + 16.x = 160
<=> 16x=160-112=48
<=>x=3
Vậy CTHH của oxit sắt là Fe2O3

gọi cthh của Oxit có dạng FexOy (xy thuộc N* )
theo bài ra ta có
x:y = 7/56 : 3/16 = 2/3
=> Cthh : Fe2O3
thử lại ptk Fe2O3 = 56.2+ 16.3 =10(đvC) (đúng với đề)

Gọi công thức hóa học của oxit sắt là: F e x O y :
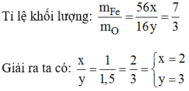
Công thức hóa học: F e 2 O 3 .

Khối lượng của các nguyên tố trong hợp chất là:
\(m_{FE}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=\dfrac{30.160}{100}=48\left(g\right)\)
Số mol có trong mỗi nguyên tố là:
\(n_{FE}=\dfrac{m_{FE}}{M_{FE}}=\dfrac{112}{56}=2\left(mol\right)\)
\(n_O=\dfrac{m_O}{M_O}=\dfrac{48}{16}=3\left(mol\right)\)
Vậy hợp chất có 2 nguyên tử Fe, 3 nguyên tử O
Công thức hóa học của hợp chất là: \(FE_2O_3\)

CTPT: FexOy
Có: \(\dfrac{m_{Fe}}{m_O}=\dfrac{56x}{16y}=\dfrac{7}{3}\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTPT: Fe2O3
Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=\dfrac{1}{8}:\dfrac{3}{16}=1:\dfrac{3}{2}=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)

\(\dfrac{m_{Fe}}{m_{O_2}}=\dfrac{7}{3}\)
\(CTĐG:Fe_xO_y\)
\(\Rightarrow x:y=\dfrac{7}{56}:\dfrac{3}{16}\)
\(=0,125:0,1875\)
\(=2:3\)
Vậy CTHH là: \(Fe_2O_3\)
CTHH: FexOy
mFe/mO = 7/3
=> 56x/16y = 7/3
=> x/y = 7/3 . 16/56 = 2/3
CTHH: Fe2O3

CTHH: FexOy
x = nFe = \(\frac{160.7}{7+3}\)/56 = 2 (mol)
y = nO = \(\frac{160.3}{7+3}\)/16 = 3 )mol)
Vậy: CTHH là Fe2O3


Gọi CTHH oxit sắt: FexOy
- Ta có: 56x+16y=160
mFe/mO=56x/16y=7/3→168x−112y=0mFemO=56x16y=73→168x−112y=0
=> x=2 và y=3
CTHH oxit sắt: Fe2O3
Sao ra dc168x vậy