Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu 5
nKMnO4=\(\dfrac{31,6.98\%}{158}\)=0,196(mol)
2KMnO4−to→K2MnO4+MnO2+O2
nO2(lt)=\(\dfrac{1}{2}\)nKMnO4=0,098(mol)
Vìhaohụt5%
⇒VO2(tt)=0,098.95%.22,4=2,08544(l)

nO2 = \(\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
pt: \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
Theo pt: \(n_{KMnO_4}=2n_{O_2}=0,6mol\)
=> nKMnO4 thực tế = 0,6:\(\dfrac{90}{100}=\dfrac{2}{3}\left(mol\right)\)
mKMnO4 = \(\dfrac{2}{3}.158=\dfrac{316}{3}g\)

\(m_{KMnO_4}=31,6.98\%=30,968g\)
\(m_{KMnO_4}=30,968.95\%=29,4196g\)
\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{29,4196}{158}=0,1862mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,1862 0,0931 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,0931.22,4=2,08544l\)
\(n_{KMnO_4}=\dfrac{31,6.98\%}{158}=0,196\left(mol\right)\\ 2KMnO_4-^{t^o}\rightarrow K_2MnO_4+MnO_2+O_2\\ n_{O_2\left(lt\right)}=\dfrac{1}{2}n_{KMnO_4}=0,098\left(mol\right)\\ Vìhaohụt5\%\\ \Rightarrow V_{O_2\left(tt\right)}=0,098.95\%.22,4=2,08544\left(l\right)\)

\(n_{Al}=\dfrac{5.4}{27}=0,2mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,2 0,15 0,1
a)\(V_{O_2}=0,15\cdot22,4=3,36l\)
b)\(n_{O_2}=0,15\cdot10\%=0,015mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,03 0,015
\(m_{KMnO_4}=0,03\cdot158=4,74g\)

PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
a) Ta có: \(n_{KMnO_4}=\dfrac{94,8}{158}=0,6\left(mol\right)\)
\(\Rightarrow n_{O_2\left(lýthuyết\right)}=0,3\left(mol\right)\) \(\Rightarrow n_{O_2\left(thực\right)}=0,3\cdot90\%=0,27\left(mol\right)\)
\(\Rightarrow V_{O_2\left(thực\right)}=0,27\cdot22,4=6,048\left(l\right)\)
b) PTHH: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PTHH: \(n_{Al_2O_3}=\dfrac{2}{3}n_{O_2}=0,18\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,18\cdot102=18,36\left(g\right)\)

a)nO2=\(\dfrac{3.36}{22.4}\)=0,15(mol)
2KMnO4(to)→K2MnO4+MnO2+O2
Theo PT: nKMnO4=2nO2=0,3(mol)
→m=mKMnO4=0,3.158=47,4(g)
b)nH2=\(\dfrac{8.96}{22.4}\)=0,4(mol)
2H2+O2(to)→2H2O
Vì \(\dfrac{nH_2}{2}\)<nO2→O2nH2 dư
Theo PT: nH2O=nH2=0,4(mol)
→mH2O=0,4.18=7,2(g)

PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
a. Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=\dfrac{1}{2}0,1=0,05\left(mol\right)\)
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=0,05.22,4=1,12\left(l\right)\)
b. PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Ta có: \(\dfrac{1}{n_{O_2}}=\dfrac{1}{0,05}\)
\(\dfrac{1}{n_{Fe}}=\dfrac{1}{0,1}\)
\(\Rightarrow\dfrac{1}{n_{O_2}}>\dfrac{1}{n_{Fe}}\)
Vậy Fe dư
Theo PTHH: \(n_{Fe_3O_4}=\dfrac{0,1.1}{3}=\dfrac{1}{30}\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4}=n_{Fe_3O_4}.M_{Fe_3O_4}=\dfrac{1}{30}.232\approx7,73g\)

$n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$2Fe +6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
$n_{SO_2} = \dfrac{3}{2}n_{Fe} = 0,3(mol)$
$n_{SO_2\ hao\ hụt} = 0,3.3\% = 0,009(mol)$
$V_{SO_2} = (0,3 - 0,009).22,4 = 6,5184(lít)$
2Fe+6H2SO4→Fe2(SO4)3+3SO2+6H2O
nFe=0,2mol
→nSO2=3/2nFe=0,3mol
→VSO2=0,3×22,4−3%=6,69l

PTHH : \(2KClO_3\rightarrow t^0\rightarrow2KCl+3O_2\uparrow\)
Số mol KClO3 tham gia phản ứng : \(n_{KClO_3}=\frac{m_{KClO_3}}{M_{KClO_3}}=\frac{12,25}{122,5}=0,1\left(mol\right)\)
1. Theo PTHH : Cứ 2 mol KClO3 tham gia phản ứng thì tạo thành 3 mol O2
=> Cứ 0,1 mol KClO3 tham gia phản ứng thì tạo thành 0,15 mol O2
=> Thể tích khí O2 thu được ở đktc là : \(V_{O_2}=n_{O_2}\times22,4=0,15\times22,4=3,36\left(l\right)\)
2. Số mol O2 tạo thành sau phản ứng : \(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{48}{32}=1,5\left(mol\right)\)
Theo PTHH : Cứ 3 mol O2 tạo thành sau phản ứng thì có 2 mol KClO3 tham gia phản ứng
=> Cứ 1,5 mol O2 tạo thành sau phản ứng thì có 1 mol KClO3 tham gia phản ứng
=> Khối lượng KClO3 cần nhiệt phân : \(m_{KClO_3}=n_{KClO_3}\times M_{KClO_3}=1\cdot126,9=126,9\left(g\right)\)
3. Số mol O2 thu được sau phản ứng ở đktc : \(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
Theo PTHH : Cứ 3 mol O2 tạo thành sau phản ứng thì có 2 mol KClO3 tham gia phản ứng
=> Cứ 0.125 mol O2 tạo thành sau phản ứng thì có 1/12 mol KClO3 tham gia phản ứng
=> Khối lượng KClO3 cần nhiệt phân : \(m_{KClO_3}=n_{KClO_3}\times M_{KClO_3}=\frac{1}{12}\cdot126,9=10.575\left(g\right)\)
Quỳnh•Sinestrea⁰⁷ : đừng làm hóa nữa, làm toàn nhầm thôi đấy
1. PTHH : \(2KClO_3-t^o->2KCl+3O_2\)
. \(n_{KClO_3}=\frac{12,25}{122,5}=0,1\left(mol\right)\)
Theo pthh : \(n_{O_2}=\frac{3}{2}n_{KClO_3}=0,15\left(mol\right)\)
=> \(V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)
2. PTHH : \(2KClO_3-t^o->2KCl+3O_2\)
\(n_{O_2}=\frac{48}{32}=1,5\left(mol\right)\)
Theo pthh : \(n_{KClO_3}=\frac{2}{3}n_{O_2}=1\left(mol\right)\)
=> \(m_{KClO_3}=1\cdot122,5=122,5\left(g\right)\)
3. PTHH : \(2KMnO_4-t^o->K_2MnO_4+MnO_2+2O_2\)
\(n_{O_2}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
Theo pthh : \(n_{KMnO_4}=n_{O_2}=0,125\left(mol\right)\)
=> \(m_{KMnO_4}=0,125\cdot158=19,75\left(g\right)\)
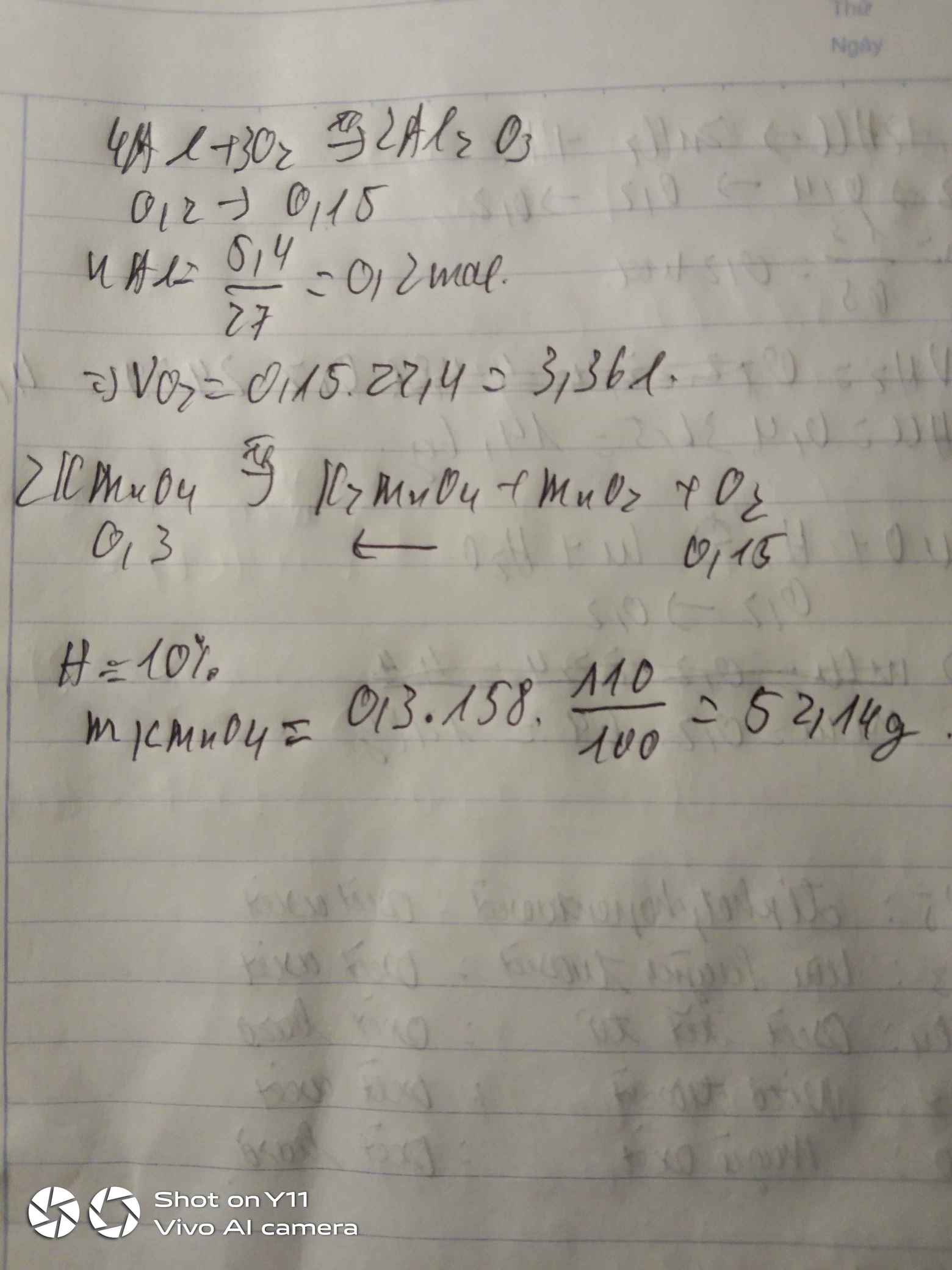
2KMnO4-to>K2MnO4+MnO2+O2
0,5------------------------------------0,25
n O2=5,6\22,4=0,25 mol
=>m KMnO4=0,5.158.20\100=12,8g