Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Hai lí do chính :
Trong lòng biển và đại dương tồn tại cân bằng hoá học :
![]()
Theo nguyên lí chuyển dịch cân bằng, khi nồng độ cacbon đioxit tăng thì cân bằng hoá học chuyển theo chiều thuận, do đó làm giảm nồng độ của cacbon đioxit.
- Sự quang hợp của cây xanh trên lục địa và của tảo ở biển và các đại dương :
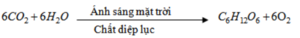
Dù cho có những quá trình tự điều tiết, khống chế sự tăng cacbon đioxit, nhưng con người đang thải lượng cacbon đioxit ngày càng nhiều hơn, vượt quá khả năng tự điều chỉnh của thiên nhiên.

Đáp án D
Phương trình phản ứng: Na 2 S 2 O 3 + H 2 SO 4 → Na 2 SO 4 + S ↓ + SO 2 ↑ + H 2 O
Nồng độ các chất phản ứng là Na2S2O3 và H2SO4 không đổi, do đó tốc độ phản ứng chỉ phụ thuộc nhiệt độ. Khi nhiệt độ tăng, tốc độ phản ứng tăng và thời gian phản ứng giảm.
Nhiệt độ ở các thí nghiệm tăng theo thứ tự sau: thí nghiệm 1 < thí nghiệm 3 < thí nghiệm 2, do đó tốc độ phản ứng thí nghiệm 1 < thí nghiệm 3 < thí nghiệm 2 và thời gian phản ứng thí nghiệm 1 > thí nghiệm 3 > thí nghiệm 2 => t 1 > t 3 > t 2 .

Đáp án D
Phương trình phản ứng: Na 2 S 2 O 3 + H 2 SO 4 → Na 2 SO 4 + S ↓ + SO 2 ↑ + H 2 O
Nồng độ chất tham gia phản ứng càng cao (nồng độ các chất trong dung dịch hỗn hợp khi trộn các chất với nhau), tốc độ phản ứng càng nhanh, thời gian kết tủa càng ngắn.
Ở đây, nồng độ dung dịch H2SO4 được giữ cố định (1 giọt), do đó trong dung dịch hỗn hợp thu được nồng độ H2SO4 không đổi, dẫn đến tốc độ phản ứng chỉ còn phụ thuộc vào nồng độ Na2S2O3.
Thứ tự tăng nồng độ Na2S2O3 trong các thí nghiệm sau: thí nghiệm 2 (12 giọt Na2S2O3 + 0 giọt H2O) > thí nghiệm 3 (8 giọt Na2S2O3 + 4 giọt H2O) > thí nghiệm 1 (4 giọt Na2S2O3 + 8 giọt H2O).
Vậy thời gian xuất hiện kết tủa theo thứ tự là t 1 > t 3 > t 2 .

Các bạn chú ý bảng của mình ở mục nhận xét chấm thi của vòng 1 nhé!
Lên rồi nhé :))